Biochemie Werkzeugkasten für die Wirkstoffentwicklung erhält Zuwachs
Die Proteinkinase Akt spielt eine zentrale Rolle bei der Entstehung von Krebs. Die unterschiedlichen Funktionen ihrer drei Isoformen sind jedoch bis heute nicht geklärt. Das liegt vor allem daran, dass geeignete biochemische und zelluläre Aufklärungsstrategien fehlen. Neue chemische Werkzeuge sollen nun dabei helfen, das Verständnis für diese Enzyme zu verbessern und damit zu wirksameren Medikamenten führen.
Anbieter zum Thema
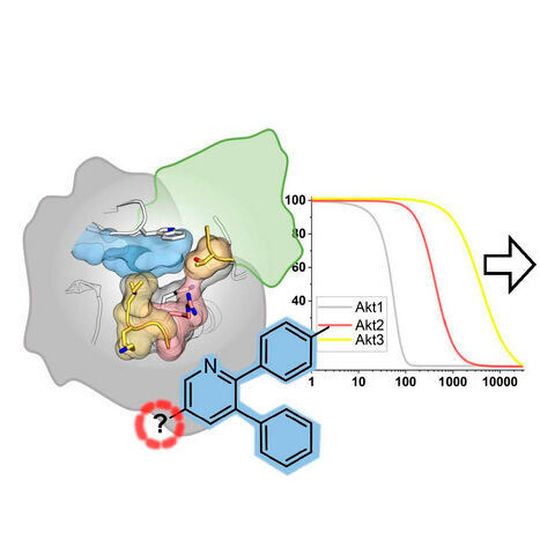
Dortmund – Die Arbeitsgruppe um Prof. Daniel Rauh von der TU Dortmund hat nun neue chemische Werkzeuge entwickelt, die das Verständnis der Akt-Isoform-spezifischen Funktionen in Gesundheit und Krankheit verbessern und die Entwicklung von Therapeutika der nächsten Generation fördern können. Die Ergebnisse wurden kürzlich in der renommierten Fachzeitschrift Nature Communications veröffentlicht.
Zelluläres Modellsystem für die Medizin
Die Forschungsgruppe, zu der auch die beiden Doktorandinnen Lena Quambusch und Laura Depta gehören, hat ein innovatives, zelluläres Modellsystem entwickelt, mit dem neuartige Akt-Isoform-selektive Inhibitoren in einer komplexen Umgebung bewertet werden können. In einem ersten Proof-of-Concept ermöglichten die so entwickelten chemischen Werkzeuge Studien zu selektiven Effekten der Akt-Hemmung in Krebszellen.
:quality(80)/images.vogel.de/vogelonline/bdb/1780300/1780393/original.jpg)
Antivirale Wirkstoffe
Nukleinsäure-Grundbaustein erstmals biokatalytisch hergestellt
Das neuartige zelluläre Modellsystem basiert auf Akt-Isoform-abhängigen Ba/F3-Zelllinien. Der strukturgeleitete Design-Ansatz gründet sich auf Pyrazinon-basierten kovalent-allosterischen Akt-Inhibitoren, die das Team um Prof. Daniel Rauh im Jahr 2019 entwickelt hatte – so genannte covalent-allosteric Akt inhibitors (CAAIs). In Kombination mit einer gründlichen Analyse der Akt-Isoform-Homologiemodelle wurde eine Reihe verschiedener und chemisch zugänglicher Pyridin-basierter CAAIs entworfen und synthetisiert. Zusätzliche Strukturdaten von zwei Akt1-Proteinkristallstrukturen im Komplex mit dieser innovativen Klasse von Inhibitoren, welche das Enzym irreversibel modifizieren und in einer inaktiven Form sperren, untermauern den Design-Ansatz. Darüber hinaus wurden quantitative kinetische Messungen durchgeführt, um die synthetisierten Verbindungen hinsichtlich ihrer Bindungseigenschaften zu untersuchen.
Neue Inhibitoren finden
Die Kombination aus biochemischer Charakterisierung, Strukturdaten und dem hier neu entwickelten zellulären System ermöglicht es, vielversprechende Inhibitoren zu identifizieren. Diese Liganden eignen sich als so genannte chemische Sonden für weitere Aufklärungsstudien und zeigen vielversprechende Ergebnisse in menschlichen Krebszellen. Gefördert wurde die Arbeit unter anderem vom Bundesministerium für Bildung und Forschung, dem Land Nordrhein-Westfalen, der Europäischen Union (Europäischer Fonds für regionale Entwicklung), dem Drug Discovery Hub Dortmund (DDHD) und dem Kompetenzzentrum KomIT.
Originalpublikation: Lena Quambusch, Laura Depta, Ina Landel, Melissa Lubeck, Tonia Kirschner, Jonas Nabert, Niklas Uhlenbrock, Jörn Weisner, Michael Kostka, Laura M. Levy, Carsten Schultz-Fademrecht, Franziska Glanemann, Kristina Althoff, Matthias P. Müller, Jens T. Siveke & Daniel Rauh: Cellular model system to dissect the isoform-selectivity of Akt inhibitors, Nature Communications volume 12, Article number: 5297 (2021); DOI: 10.1038/s41467-021-25512-8
(ID:47629153)






:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d8/94/d8946bebf210c5826a6bfd51d610eedc/0130122950v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ce/d1/ced1a66ddc5248ac5c86aa873b3c8d5a/0131387387v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ba/32/ba322cc757f2f82da2839729e0648ca0/0131377715v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/7a/3e/7a3e9478433a525b34c6b34a0aab133f/0131322665v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/14/59/14590acbf17f99545741a47daa2c66e1/5u3a3997-6720x3778v1.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/69/ba/69ba64e74eade/ratiolab-logo.png)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/125600/125653/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/121500/121544/65.png)
:quality(80)/p7i.vogel.de/wcms/d4/d8/d4d8afb0f22f350562e0b575c88b084f/0125541248v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/de/1b/de1bbdc86c6dfd2c2f3fe970ada78c55/0126310547v1.jpeg)