Enzyme Biochemiker lösen Rätsel in der Evolution von Enzymen
Anhand von tRNA-Nukleotidyltransferasen – Enzymen, die aus einzelnen Bausteinen (Nukleotiden) Ribonukleinsäuren aufbauen bzw. vervollständigen können ist Forschern nun ein entscheidender Fortschritt hin zum Verständnis der Evolution von Enzymen gelungen.
Anbieter zum Thema
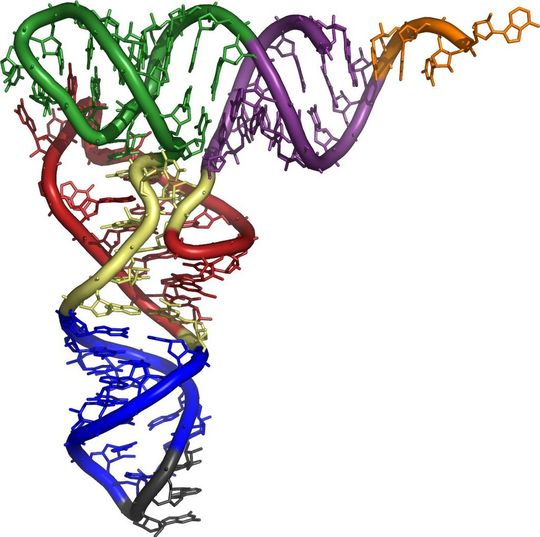
Leipzig – Wissenschaftler um Biochemiker Prof. Dr. Mario Mörl vom Institut für Biochemie der Universität Leipzig konnten kürzlich Aufbau und Funktion eines sogenannten A-addierenden Enzyms aufklären – ein Enzym, das ganz gezielt einen einzelnen Nukleotid-Baustein (Adenosinmonophosphat oder kurz „A“) an tRNAs heftet. Erstmals erklären sie, warum diese Enzyme trotz ihrer Ähnlichkeit zu komplexeren Nukleotidyltransferasen nur diese eingeschränkte Reaktion katalysieren können.
tRNA-Nukleotidyltransferasen heften drei Nukleotidbausteine (zwei Cytidinmonophosphate, kurz „C“, und ein Adenosinmonophosphat, „A“) in der Reihenfolge C-C-A an tRNA-Moleküle und generieren dabei die Position, an der tRNAs mit Aminosäuren beladen werden – eine essenzielle Voraussetzung bei der Synthese von Proteinen in der Zelle. Zunächst war es ein interessantes Phänomen, das Professor Mörl so beschreibt: „Einige dieser Enzyme können nicht die komplette Sequenz C-C-A synthetisieren, sondern sind auf den Einbau der beiden C-Positionen (CC-addierende Enzyme) bzw. der A-Position (A-addierende Enzyme) spezialisiert. Beide Enzymtypen sehen jedoch auf den ersten Blick gleich aus, sodass nicht klar war, woher diese Spezialisierung kommt.“ In einer vorangegangenen PNAS-Veröffentlichung (2008) konnten die Forscher bereits klären, weshalb die CC-addierenden Enzyme kein A einbauen können. Bei den A-addierenden Enzymen war dies jedoch deutlich schwieriger: Strukturell gesehen besitzen diese Enzyme alle Komponenten, die nötig sind, um eine komplette C-C-A-Sequenz an tRNAs zu heften.
Variable Region erlaubt evolutionäre Veränderung der Enzym-Funktionalität
Aktuell ging es somit um die Frage: „Wenn diese Enzyme alle Elemente zur C-C-A-Addition tragen, warum können sie dann lediglich einen einzelnen A-Rest einbauen?“. Die Leipziger Biochemiker entfernten dazu sukzessive immer größere Teile von A-addierenden Enzymen und testeten die entstandenen verkürzten Varianten auf ihre Aktivität. Dabei zeigte sich, dass eine kleine Region dafür verantwortlich ist, dass die A-addierenden Enzyme eine eingeschränkte Funktionalität besitzen. Entfernte man diese Region, so konnten die Enzyme tatsächlich komplette C-C-A-Sequenzen synthetisieren. Die inhibitorische Wirkung dieser Region scheint darin zu liegen, dass über sie reguliert wird, welche tRNAs vom Enzym erkannt werden – nämlich nur noch tRNAs, die bereits die Sequenz C-C erhalten haben und denen somit nur noch das letzte A fehlt. Der Bereich, in dem sich diese Region befindet, ist in der Evolution überraschend variabel und kaum konserviert. Die erhaltenen Daten weisen darauf hin, dass diese Region offenbar von der Natur genutzt wurde, um im Lauf der Evolution die Funktionalität dieser Enzyme zu verändern und sie mit neuen Eigenschaften auszustatten.
Originalveröffentlichung: Tretbar, S., Neuenfeldt, A., Betat, H., and Mörl, M. (2011). An inhibitory C-terminal Region dictates the Specificity of A-adding Enzymes. Proc. Natl. Acad. Sci. USA 108, No. 52, 21040-21045.
(ID:31898270)






:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d8/94/d8946bebf210c5826a6bfd51d610eedc/0130122950v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0131240119v5.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/4c/3c4c43bf567ff12c14920f6a8990edcb/0131229738v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3d/c2/3dc269b3435d97799061920f4a281393/0131172010v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fe/3e/fe3e220cf6ac0f453fc75187c04572fd/0130535166v2.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/131900/131910/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/126900/126940/65.png)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/84700/84716/65.jpg)
:quality(80)/p7i.vogel.de/wcms/0c/14/0c14ef9b2172311c0c58ed4b9c1c0276/0127427218v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/03/bb032ceb9559ab36fc68e0becfd96de9/0130195320v2.jpeg)