Katalysemechanismen aufklären Molekül-GPS liefert Enzymbilder
Enzyme katalysieren zahlreiche biologische Reaktionen. Wie die Makromoleküle genau arbeiten, ist aufgrund ihrer komplexen Struktur schwer zu untersuchen. Ein neues Aufnahmeverfahren von Forschern der Universität Bonn bringt nun neue Einblicke in die Funktion von Enzymen. Warum das Verfahren Ähnlichkeiten zu einem GPS hat, erfahren Sie in diesem Beitrag.
Anbieter zum Thema

Bonn – Wenn Wissenschaftler die Arbeitsweise eines Enzyms nachvollziehen wollen, stellt dies eine große Herausforderung dar: Sofern sie überhaupt die Struktur des Moleküls kennen, dann meist nur als eine Momentaufnahme, sozusagen ein Standbild. Wie sich das Enzym in Aktion verhält, welche Teile sich aufeinander zu und welche voneinander wegbewegen, können sie aus einer einzelnen Aufnahme nicht erkennen.
Enzyme katalysieren in den Zellen bestimmte chemische Reaktionen. Dies erfolgt an bestimmten Stellen des Enzyms, den Katalytischen Zentren, an die der Ausgangsstoff der jeweiligen Reaktion andockt. „Während dieses Vorgangs ändert sich in der Regel die dreidimensionale Form des Enzyms“, sagt Prof. Dr. Olav Schiemann vom Institut für Physikalische und Theoretische Chemie der Universität Bonn. „Im Normalfall lassen sich diese Konformationsänderungen nicht oder nur mit großem Aufwand sichtbar machen. Das macht es oft schwierig, den Katalyse-Mechanismus nachzuvollziehen.“
Schiemanns Arbeitsgruppe hat nun aber eine Methode entwickelt, mit der die Bewegungen von Teilen des Proteins gegeneinander im Laufe der Katalyse gemessen werden können. Die Bonner Wissenschaftler arbeiten schon seit einigen Jahren an derartigen Verfahren. In ihrer aktuellen Studie haben sie eine besonders wichtige Gruppe von Enzymen unter die Lupe genommen. Diese tragen in ihren katalytischen Zentren Metallionen mit zahlreichen ungepaarten Elektronen. Ein Beispiel ist das Hämoglobin, das mithilfe eines Eisen-Ions Sauerstoff bindet und so mit dem Blut transportieren kann.
Flippende Ionen
„Unsere gängigen Methoden sind für derartige Hochspin-Ionen ungeeignet“, sagt Schiemanns Mitarbeiter Dr. Dinar Abdullin. „Wir haben daher ein neues Verfahren entwickelt, die Theorie dazu ausgearbeitet und mit Erfolg getestet.“ Die Forscher nutzten dazu die Tatsache, dass Hochspin-Ionen sich wie kleine Elektromagnete verhalten. Zudem können sie zufällig ihre Polung ändern – sie „flippen“: Der Nordpol wird zum Süd- und der Süd- zum Nordpol.
Dieses Phänomen lässt sich für die Abstandsmessung nutzen. Dazu verknüpfen die Wissenschaftler das Enzym mit bestimmten chemischen Verbindungen, die ebenfalls elektromagnetische Eigenschaften haben. „Wenn die Hochspin-Ionen flippen, reagieren diese kleinen Elektromagnete auf das veränderte Magnetfeld in ihrer Umgebung, indem sie ebenfalls ihre Polung ändern“, erklärt Abdullin. Wann und wie sie das machen, hängt u.a. von der Entfernung zum Hochspin-Ion ab. Die Distanz zwischen den beiden lässt sich deshalb über die Frequenz des Flippens genau bestimmen.
Molekulares GPS
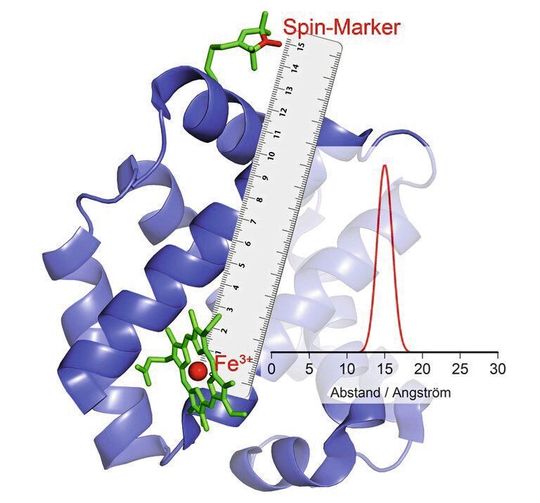
Wenn man mehrere Magnetgruppen an ein Enzym bindet, erhält man auf diese Weise den Abstand jeder dieser Gruppen zum Hochspin-Ion und damit zum katalytischen Zentrum. „Durch Kombination dieser Werte können wir, wie mit einem molekularen GPS, die räumliche Position dieses Zentrums messen“, erklärt Schiemann. „Wir können so zum Beispiel feststellen, wie sich seine Lage im Verlauf der Katalyse relativ zu den anderen Magnetgruppen ändert.“
Dem Enzym wirklich bei der Arbeit zusehen können die Wissenschaftler aber noch nicht. „Momentan arbeiten wir noch mit tiefgekühlten Zellen“, sagt Schiemann. „Diese enthalten zahlreiche Enzyme, die zu unterschiedlichen Zeitpunkten der katalytischen Reaktion eingefroren wurden. Wir erhalten also keinen Film, sondern eine Reihe von Standbildern.“
:quality(80)/images.vogel.de/vogelonline/bdb/1363100/1363113/original.jpg)
Körpereigener Giftcocktail
Filmischer Beweis: Unser Immunsystem nutzt Chlorbleiche zum Abtöten von Bakterien
„Wir arbeiten aber schon an der nächsten Verbesserung“, betont der Chemiker: „Der räumlichen Vermessung von Biomolekülen in Zellen und bei Raumtemperatur.“ Die Forscher erhoffen sich so auch Einblicke in die Entstehung bestimmter Erkrankungen, die durch Funktionsstörungen von Enzymen ausgelöst werden. An der Studie waren neben Dr. Maxim Yulikov von der ETH Zürich von Seiten der Universität Bonn auch die Arbeitsgruppe um Prof. Dr. Stefan Grimme (ebenfalls Institut für Physikalische und Theoretische Chemie) sowie von Prof. Dr. Arne Lützen (Kekulé-Institut) beteiligt.
D. Abdullin, H. Matsuoka, M. Yulikov, N. Fleck, C. Klein, S. Spicher, G. Hagelueken, S. Grimme, A. Lützen und O. Schiemann: Pulsed EPR Dipolar Spectroscopy under the Breakdown of the High-Field Approximation: The High-Spin Iron(III) Case. Chem. Eur. J. 2019; DOI: 10.1002/chem.201900977
(ID:45910186)






:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d8/94/d8946bebf210c5826a6bfd51d610eedc/0130122950v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ce/d1/ced1a66ddc5248ac5c86aa873b3c8d5a/0131387387v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ba/32/ba322cc757f2f82da2839729e0648ca0/0131377715v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/7a/3e/7a3e9478433a525b34c6b34a0aab133f/0131322665v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/14/59/14590acbf17f99545741a47daa2c66e1/5u3a3997-6720x3778v1.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/115900/115965/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/86900/86921/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/84700/84716/65.jpg)
:quality(80)/p7i.vogel.de/wcms/c6/3c/c63c199d11fa5a7a632001eb2408122a/0125884875v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/0c/14/0c14ef9b2172311c0c58ed4b9c1c0276/0127427218v2.jpeg)