Miniaturisierte Hochdurchsatz-Methode „Nano-Fleming“: Neue Antibiotika auch auf unserer Haut?
Neue Antibiotika sind im Zeitalter zunehmender Resistenzen mehr als gefragt. Nun haben Schweizer Forscher eine viel versprechende Methode entwickelt, mit der sie schnell eine sehr große Anzahl an Molekülen auf ihre antibiotische Wirkung hin testen können. Dazu haben sie die Methode des Penicillin-Entdeckers Alexander Fleming modernisiert und miniaturisiert.
Anbieter zum Thema
Zürich/Schweiz – Die Geschichte der Entdeckung des Penicillins durch Alexander Fleming ist auch eine Geschichte des Zufalls: Unbeabsichtigt gelangte vor 90 Jahren ein Schimmelpilz auf eine Bakterienkultur in Flemings Labor. Der schottische Bakteriologe beobachtete, dass der Pilz einen Stoff produzierte, der die Bakterien auf der Zellkulturplatte abtötete. Er entdeckte so Penicillin, eines der ersten Antibiotika.
Antibiotika – stumpfer werdende Wunderwaffe
Mittlerweile gibt es mehrere Dutzend Klassen von Antibiotika. Ein Großteil dieser Medikamente sind Naturstoffe oder bauen auf diesen auf. Und noch immer ist die Nachweismethode dieselbe wie zu Flemings Zeiten: Ein Antibiotikum ist ein Stoff, der auf einer Zellkulturplatte Bakterien abzutöten vermag.
Und die Wissenschaft sucht weiterhin unermüdlich nach neuen antimikrobiellen Wirkstoffen. Denn jahrzehntelanger nahezu exzessiver und z.T unsachgemäßer Gebrauch der Antibiotika, lassen immer mehr Vertreter dieser einst als Wunderwaffe gepriesenen Wirkstoffe unwirksam werden: Antibiotikaresistenzen sind weltweit auf dem Vormarsch und und fordern schon heute Tausende Todesopfer.
Hochdurchsatz-Analyse: Flemings Methode im Miniformat
Wissenschaftler um Steven Schmitt aus der Gruppe von ETH-Professor Sven Panke am Department für Biosysteme der ETH Zürich in Basel haben nun Flemings Methode modernisiert und miniaturisiert und sie so fit gemacht für die Hochdurchsatz-Analyse von Mikroorganismen und den von ihnen produzierten Wirkstoffen. „Während es heute mit herkömmlichen Methoden bis zu einem Jahr dauert, um 10.000 Wirkstoffproduzenten zu testen, können wir innerhalb von wenigen Tagen Millionen von Varianten untersuchen“, sagt Schmitt, der die Methode in seiner Doktorarbeit an der ETH entwickelte.
Mit der neuen Technologie ist es den ETH-Wissenschaftlern gemeinsam mit niederländischen und deutschen Kollegen gelungen, eine Reihe neuer Antibiotika-Kandidaten zu identifizieren. Nun werden die Forscher in einem nächsten Schritt untersuchen, ob sich unter diesen Kandidaten auch solche befinden, die sich für eine Anwendung in der Medizin eignen.
„Bubble Tea“ für die Wirkstoffsuche
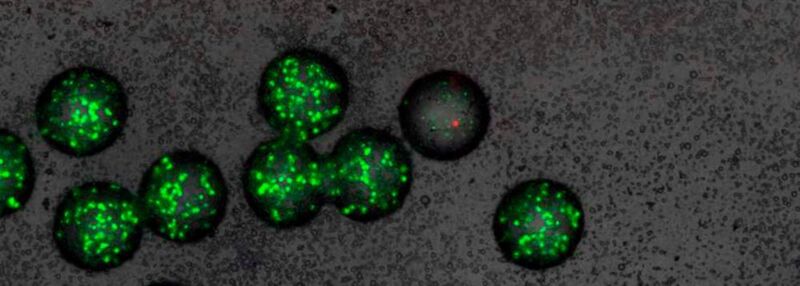
Was bei Alexander Fleming eine Zellkulturschale mit einem Durchmesser von zehn Zentimetern war, sind in der neuen, „Nano-Fleming“ genannten Technik kleine Gel-Kügelchen von bloß einem halben Millimeter – ähnlich wie „Bubble Tea“ oder Kaviar-Imitat aus der Molekularküche. In diesen Kügelchen können die Wissenschaftler neue Stoffe auf ihre antibiotische Wirkung hin testen. Sie betten dazu in die Kügelchen einerseits mehrere Sensor-Bakterien ein und andererseits pro Kügelchen jeweils einen Mikroorganismus, der einen zu testenden und potenziell antibiotisch wirkenden Stoff produziert.
Wirkt der produzierte Stoff tatsächlich antibiotisch, sterben die Sensor-Bakterien ab. Wirkt er nicht, vermehren sie sich und bilden Zellhaufen. Nachdem die Wissenschaftler die Sensor-Bakterien mit einem Fluoreszenz-Farbstoff markieren, können sie die nur schwach fluoreszierenden Gel-Kügelchen mithilfe einer Hochdurchsatz-Sortierungsmethode aussortieren. In ihnen befindet sich ein Mikroorganismus, der ein wirksames Antibiotikum produzierte. Anschließend können die Wissenschaftler diesen Wirkstoff identifizieren.
Wirksamere Antibiotika
In der aktuellen Arbeit, welche die Forscher im Fachmagazin Nature Chemical Biology veröffentlichten, testeten sie eine Sammlung von 6000 Peptiden auf ihre antibiotische Wirkung. Es handelte sich dabei um Moleküle, die einer Gruppe von bekannten Peptid-Antibiotika, sogenannten Lantibiotika, ähnlich sind. Die Wissenschaftler wollten untersuchen, ob es durch eine intelligente Veränderung der molekularen Struktur der Lantibiotika möglich ist, ihre Wirksamkeit zu erhöhen oder bekannte Resistenzmechanismen zu umgehen.
:quality(80)/images.vogel.de/vogelonline/bdb/1371800/1371844/original.jpg)
Cocktail aus 45 Antibiotika
Resistenzen unbekannt: Bienenwölfe nutzen seit 68 Millionen Jahren erfolgreich die gleichen Antibiotika
Zusammen mit den niederländischen und deutschen Kollegen gingen sie von bekannten Lantibiotika und ihren strukturellen und funktionellen Untereinheiten aus. In einem biotechnologischen Ansatz kombinierten sie die Untereinheiten verschiedener Lantibiotika auf alle erdenklichen Weisen und fertigten so eine Sammlung von Mikroorganismen an, welche diese neukombinierten Peptide herstellen. Diese Mikroorganismen testeten sie anschließend mit der „Nano-Fleming“-Methode. Tatsächlich fanden sie elf Peptide, die im Vergleich zu den bekannten Lantibiotika entweder in kleinerer Dosis wirken oder in der Lage sind, bekannte Resistenzmechanismen auszutricksen.
Wirkstoff-Suche in der Natur
„Mit der Methode lässt sich auch hervorragend untersuchen, ob Mikroorganismen aus der Natur bisher unentdeckte Wirkstoffe produzieren“, sagt Schmitt. Dass Mikroben versuchten, ihre Konkurrenten mit biochemischen Verbindungen auszuschalten, sei ein natürlicher und verbreiteter Mechanismus. Möglicherweise finde man daher in Lebensräumen wie Bodenproben oder dem noch wenig untersuchten Mikrobiom auf der menschlichen Haut und im Speichel neue Antibiotikaklassen.
Mit der neuen Technik könnten Mikroorganismen aus diesen Lebensräumen sehr gut analysiert werden. „Und weil wir nun in kurzer Zeit sehr viel mehr Wirkstoffproduzenten testen können als mit bisherigen Methoden, erhöht sich die Chance, Wirkstoffe von seltenen Mikroorganismen zu entdecken.“
Ebenso könnte die Technik angepasst werden, um weitere Kriterien für Antibiotika gleich bei der ersten Analyse zu testen, etwa die Stabilität in der menschlichen Blutbahn oder die Umgehung von Resistenzmechanismen. Oder es wäre möglich, die Gel-Kügelchen mit verschiedenen Sensor-Bakterien zu bestücken – solchen, die ein Wirkstoff unbedingt abtöten soll, zum Beispiel Krankheitserregern, und anderen, denen er keinesfalls schaden soll, beispielsweise Bakterien der gesunden Haut- oder Mundflora.
Weiterentwicklungen wie diese plant Schmitt nun im Rahmen seines ETH-Pioneer-Fellowships sowie eines Bridge-Stipendiums, mit dem der Schweizerische Nationalfonds und Innosuisse gemeinsam Entwicklungen an der Schnittstelle von Hochschulen und Industrie fördert. Ebenfalls in Planung ist die Gründung eines Spin-offs, um die Methode zu kommerzialisieren.
Originalpublikation: Schmitt S, Montalbán-López M, Peterhoff D, Deng J, Wagner R, Held M, Kuipers OP, Panke S: Analysis of modular bioengineered antimicrobial lanthipeptides at nanoliter scale. Nature Chemical Biology 2019, 15: 437, doi: 10.1038/s41589-019-0250-5
* Dr. F. Bergamin: ETH Zürich, 8092 Zürich/Schweiz
(ID:45896347)






:quality(80)/p7i.vogel.de/wcms/a1/66/a166ebdbf76639663c4fe76086c2c5b6/0130751325v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/fe/3e/fe3e220cf6ac0f453fc75187c04572fd/0130535166v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/de/74/de74b5de1a05065fd65e37f9818b0154/0130573678v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/46/10/46104916e8a69933218fded0d5925feb/0130443323v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0130924147v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a6/e0/a6e0ab14cf7f6b22d536f6ca6e5fb777/0130793394v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/df/3d/df3d3f7d7b425eabae87bab4ef68bd6c/0130259765v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/b9/32/b9326aa0b6f26d5e5eeee82c86aab8b6/0130976290v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/2d/5f/2d5f14d92ec22f38682c6d240600579f/0131000090v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/19/40/194054b15f3c0e161583d7ea8917ec3f/0130974372v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/e2/5e/e25e2c9f40617e17d32524787c6ece1d/0130248690v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/09/88/09883aaf7db3151a2e894d56c2a515d4/0130982666v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/2e/17/2e1795b6750cc3eaad6ba81c0bc79d16/0100811496v7.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/115900/115965/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/69800/69835/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/67/49/6749e1ed03ca4/spt-logo-pink-black-01--2-.png)
:quality(80)/p7i.vogel.de/wcms/de/1b/de1bbdc86c6dfd2c2f3fe970ada78c55/0126310547v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/0d/e2/0de2ad009e7d7da55cddbe296a647495/0129265791v2.jpeg)