Neue Antibiotikaklasse untersucht Energieversorgung von multiresistenten Keimen kappen
Der Kampf gegen multiresistente Keime wird Jahr für Jahr schwieriger, weil die Auswahl an noch wirksamen Antibiotika sinkt. Neue Wirkstoffe sind daher besonders stark gefragt. Nun haben Forscher der Universität Tübingen eine vielversprechende neue Antibiotikaklasse untersucht und herausgefunden, nach welchem Mechanismus diese Wirkstoffe die Bakterien besiegen.
Anbieter zum Thema

Tübingen – Ein Forschungsteam der Universitäten Tübingen und Göttingen sowie des Deutschen Zentrums für Infektionsforschung hat die Wirkungsweise einer neuen Klasse von Antibiotika untersucht, die gegen multiresistente Krankheitserreger hochwirksam ist. Wie Dr. Nadine Schilling vom Institut für Organische Chemie der Universität Tübingen herausfand, beeinträchtigen so genannte Fibupeptide die Energieversorgung der Bakterienzelle, was zu deren Tod führt.
Bereits 2016 hatten Tübinger Wissenschaftler ein erstes Fibupeptid entdeckt, das von unserem Mikrobiom selbst gebildet wird. Die Wissenschaftler nannten den Stoff Lugdunin, nach seinem Produzenten, dem Bakterium Staphylococcus lugdunensis, das die menschliche Nasenschleimhaut besiedelt.
Lugdunin hat eine ungewöhnliche chemische Struktur und ist damit möglicherweise ein Prototyp für eine völlig neue Klasse von Antibiotika. Es wirkt unter anderem gegen die für Menschen besonders gefährlichen Methicillin-resistenten Bakterien der Art Staphylococcus aureus (MRSA). Besonders gefürchtet ist MRSA in Kliniken, da er häufig immungeschwächte Patienten befällt. Nach einer im November 2018 veröffentlichten Studie gab es in der EU allein im Jahr 2015 rund 670.000 Infektionen durch multiresistente Erreger, an deren Folgen 33.000 Patienten starben.
Wie wirkt das neue Antibiotikum?
Die Forscher haben nun verschiedene Lugdunin-Substanzen mittels chemischer Synthese produziert und die für die Wirkung von Lugdunin notwendigen chemischen Strukturelemente bestimmt. Damit haben sie Hinweise auf den Wirkmechanismus des Antibiotikums erhalten. „Jede Bakterienzelle braucht zum Leben eine so genannte Transmembranspannung“, sagt Schilling. „Das heißt, für den Krankheitserreger ist es entscheidend, dass sich die Konzentrationen elektrisch geladener Teilchen im Inneren der Zelle und im umgebenden Milieu unterscheiden.“ Fibupeptide wie Lugdunin sind dazu in der Lage, positiv geladene Wasserstoffionen durch die Membran zu transportieren und den Ladungsunterschied aufzuheben. „Dadurch kommt es zu einer Art Energiestillstand“, sagt die Forscherin. Die Folge davon: Die Bakterienzelle stirbt.
:quality(80)/images.vogel.de/vogelonline/bdb/1556800/1556872/original.jpg)
Miniaturisierte Hochdurchsatz-Methode
„Nano-Fleming“: Neue Antibiotika auch auf unserer Haut?
Besondere Struktur von Lugdunin
Die Entwicklung von Antibiotikaresistenzen macht die Behandlung von bakteriellen Infektionen zunehmend schwieriger. Viele der zurzeit verwendeten neuen Antibiotika unterscheiden sich nur geringfügig von solchen, gegen die schon mehrere Resistenzen bekannt sind. Es ist daher gut möglich, dass auch jene neuen Medikamente in kurzer Zeit unwirksam werden. „Daher ist das Interesse an neuen antibiotischen Strukturen wie dem Lugdunin und deren Wirkungsweise enorm“, betont Stephanie Grond, Professorin für Organische Chemie und Naturstoffforschung an der Universität Tübingen.
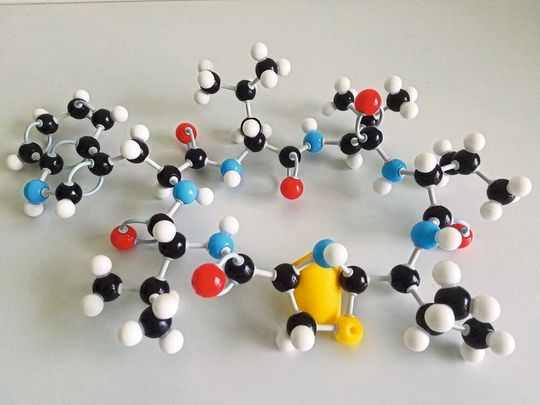
Lugdunin habe eine einzigartige chemische Struktur, sagt Grond. Es besteht aus einem Ring von Aminosäurebausteinen (eine Peptidstruktur), in den eine charakteristische ringförmige Schwefel-Stickstoffverbindung, Thiazolidin genannt, wie eine Schmuck-Schnalle eingebaut ist. Schnalle heißt auf Latein fibula, daher erhielt die neue Stoffklasse den Namen Fibupeptide. Der besondere Thiazolidinring gehört zu den Bausteinen im Lugdunin, die für die antibakterielle Wirkung unverzichtbar sind.
Spiegelbild mit gleicher Wirkung
Um die für die antibiotische Wirkung notwendigen Strukturen des Lugdunins zu identifizieren, hat das Forschungsteam eine Vielzahl von Abkömmlingen hergestellt. Nach und nach wurden Teile der chemischen Struktur verändert und jeweils die antibiotische Aktivität bestimmt. „Viele bisher bekannte Peptidantibiotika wirken in der Regel sehr spezifisch“, sagt Schilling. Beispielsweise könnten sie sich durch ihre räumliche Struktur an ein Enzym binden, notwendige Prozesse blockieren und so die Entstehung neuer Bakterienzellen verhindern. Das ist beim Lugdunin anders, wie vor allem ein Test mit seinem strukturellen Spiegelbild ergab.
„Einen Stoff und sein strukturelles Spiegelbild kann man sich vorstellen wie eine rechte und eine linke Hand, die nicht deckungsgleich sind. Die linke Hand passt nicht in einen rechten Handschuh, daher wirken die spiegelverwandten Stoffe räumlich nicht gleich“, erklärt die Forscherin. „Beim gespiegelten Lugdunin, das mittels chemischer Synthese produziert wurde, blieb jedoch dessen antibiotische Wirkung erhalten. Wir konnten also ausschließen, dass sie auf einer räumlichen Interaktion beruht.“ Für die Resistenzentwicklung ist das Fehlen einer solchen räumlichen Interaktion vorteilhaft, und Resistenzen gegenüber Lugdunin konnten in Laborversuchen bisher nicht erzeugt werden.
Klinische Studien in Planung
Um zu klären, ob sich die Fibupeptide zukünftig als Wirkstoffkandidaten für die therapeutische Anwendung eignen, werden in Zukunft umfangreiche präklinische und klinische Studien erforderlich sein. Ob Lugdunin und verwandte Stoffe in Zukunft wirksam und sicher zur Behandlung von Infektionen mit multiresistenten Keimen eingesetzt werden können, wollen die beteiligten Forscher unter anderem im Rahmen des seit Anfang 2019 laufenden Tübinger Exzellenzclusters „Kontrolle von Mikroorganismen zur Bekämpfung von Infektionen“ herausfinden.
Originalpublikation: Nadine A. Schilling, Anne Berscheid, Johannes Schumacher, Julian S. Saur, Martin C. Konnerth, Sebastian N. Wirtz, José M. Beltrán-Beleña, Alexander Zipperer, Bernhard Krismer, Andreas Peschel, Hubert Kalbacher, Heike Brötz-Oesterhelt, Claudia Steinem, Stephanie Grond: Synthetic Lugdunin Analogues Reveal Essential Structural Motifs for Antimicrobial Action and Proton Translocation Capability, Angewandte Chemie (2019); DOI: 10.1002/anie.201901589
* Dr. K. G. Rijkhoek, A. Karbe, Eberhard Karls Universität Tübingen, 72074 Tübingen
(ID:45958243)






:quality(80)/p7i.vogel.de/wcms/c9/16/c9162be8c6014187286dda23e57f8793/0130654555v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/9f/9d/9f9d6fc46606d654deca536f05102f7a/0130752952v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/58/bb58da17d7bb11b44fcae8d06c35df76/0130791510v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/0f/0c/0f0c5774037cc09a3536d24702f6204b/0130936383v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0130924147v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a6/e0/a6e0ab14cf7f6b22d536f6ca6e5fb777/0130793394v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/63/85/638523e67603079a004bbd3a99b6ad92/0130856502v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/2d/5f/2d5f14d92ec22f38682c6d240600579f/0131000090v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/19/40/194054b15f3c0e161583d7ea8917ec3f/0130974372v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/5a/25/5a251d7c5cce7101518c9b16850267f1/0130561986v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/5d/5d/5d5de6cfa0d711a690b108f9a29bad35/0130932970v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/09/88/09883aaf7db3151a2e894d56c2a515d4/0130982666v2.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/68/87/688727a5ba8d5/logo-dr-weigert--de-hygiene-mit-system-200-.png)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/86900/86921/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/69/a7/69a7ea89887e5/thg-logo-oclaim-rgb.png)
:quality(80)/p7i.vogel.de/wcms/18/d9/18d9283f0c3e897e0e0a3c155496bebc/0125083957v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/de/13/de1394793148b40f1e38c630c4e22d4e/0126944226v2.jpeg)