Photokatalysatoren im molekularen Korsett Gerüstet für Treibstoff aus Sonnenlicht
Energie aus Sonnenlicht gewinnen – ein wichtiger Beitrag zur Energiewende. Um Lichtenergie zu speichern, eignet sich die photokatalytische Wasserspaltung. Wir haben in unserer „Live im Labor“-Reihe ein Forscherteam an der Universität Würzburg besucht, das molekulare Gerüste baut, um Photokatalysatoren noch effizienter zu machen.
Anbieter zum Thema

Nur eine Stunde. In dieser Zeit strahlt die Sonne mehr Lichtenergie auf die Erde ein als der Weltenergiebedarf eines ganzen Jahres. Nur leider läuft unsere technisierte Welt nicht mit Licht, sondern noch immer zu großen Teilen mit Kohle und Benzin. Eine gefährliche Abhängigkeit, wie uns in der Vergangenheit bereits schmerzhaft verdeutlicht wurde. „Die Ölkrise in den 1970er Jahren hat viele Wissenschaftler auf dem Gebiet der regenerativen Rohstoffe und Energiequellen hervorgebracht. Heute gehen diese allmählich alle frustriert in den Ruhestand, weil noch immer keine Ablöse des Öls erfolgt ist“, sagt Prof. Dr. Frank Würthner von der Universität Würzburg. Er ist Teil einer neuen Generation von Forschern, die die Arbeit ihrer Vorgänger aufgenommen hat und neue Wege erprobt, Lichtenergie in nutzbare Kraftstoffe umzuwandeln und der Abhängigkeit fossiler Energieträger zu entkommen.

Seit 2002 hat Würthner den Lehrstuhl Organische Chemie II an der Universität Würzburg inne. Der 55-Jährige forscht dort mit zurzeit sechs Leuten seines rund 50 Personen starken Teams an der photokatalytischen Wasserspaltung – ein Prozess, mit dem sich die Energie des Sonnenlichts in Form von Wasserstoffgas speichern lässt und der in Zukunft ein wesentlicher Bestandteil unserer nachhaltigeren Energieversorgung werden könnte. „Wenn man Licht zur Energiegewinnung nutzen möchte, gibt es prinzipiell zwei Ansätze: Photovoltaik, wobei man Licht in elektrischen Strom umwandelt, oder aber die artifizielle Photosynthese, bei der Lichtenergie in Form von chemischer Energie gespeichert wird“, erklärt Würthner. Seine Arbeitsgruppe verfolgt den zweiten Ansatz. Sie hat sich zum Ziel gesetzt, die Grundlagen der photokatalytischen Wasserspaltung zu erforschen und damit den Weg für effizientere Katalysesysteme zu ebnen. Denn ohne leistungsstarke Photokatalysatoren kann die Sonne noch so lange auf ein Glas Wasser scheinen, Wasserstoff entsteht dabei nicht. Erst mit dem richtigen Katalysator reicht die Lichtenergie der Sonnenstrahlung, um die Bindungen der Wassermoleküle aufzubrechen.
Organische Chemie und Photokatalyse vereint
Damit dies mit bereits etablierten Photokatalysatoren noch besser gelingt, arbeitet die Würthner-Gruppe an deren Feintuning. Dies ist auch eine Aufgabe von Ana-Lucía Meza. Die aus Peru stammende Forscherin hat an der Universität Heidelberg ihren Master in Organischer Chemie gemacht und ist 2016 gemeinsam mit ihrer Kollegin Dorothee Schindler für die Promotion in den Arbeitskreis von Würthner nach Würzburg gekommen. „Mit Photokatalyse hatte ich vorher gar nichts zu tun. Ich habe in Heidelberg Käfigmoleküle und ausgedehnte Pi-Systeme synthetisiert. Für meine Doktorarbeit wollte ich aber gerne etwas mit einer konkreten Anwendung machen. Hier kann ich jetzt meine Erfahrungen zur Organischen Synthese mit der Photokatalyse verknüpfen.“
Die beiden Doktorandinnen arbeiten in der Würthner-Gruppe mit Ruthenium-Katalysatoren. „Das sind momentan die effizientesten“, sagt Meza. Doch was bringen da ihre Synthesekenntnisse der organischen Chemie, wenn die Photokatalyse an anorganischen Metallzentren stattfindet? „Die Rutheniumatome sind zwar für die eigentliche Katalyse verantwortlich. Aber was wir uns gedacht haben ist: Wir können viele von diesen kleinen Systemen, die schon für sich effizient sind, in ein großes Molekül zusammenbringen – ein Makromolekül –, sodass sie miteinander arbeiten und noch effizienter werden.“
Warum aber sollte man überhaupt den Umweg auf sich nehmen, Wasser in Sauerstoff und den chemischen Energiespeicher Wasserstoff zu zerlegen, statt das Sonnenlicht direkt in Photovoltaikanlagen zu verstromen? Schließlich nagt jeder zusätzliche Umwandlungsschritt an der Wirkungsbilanz. Eine Antwort ist draußen am Himmel zu sehen – oder eben nicht: Die Sonne. Wenn sie scheint, liefern moderne Siliziumsolarzellen in Deutschland schon heute ausreichend Strom, um 8,7% des Nettostromverbrauchs zu decken. Dies geht aus einem Bericht des Fraunhofer Instituts für Solare Energiesysteme hervor [1]. Doch bei schlechtem Wetter ist auch die Stromausbeute schlecht. Es geht also nicht nur darum, Strom aus Licht zu erzeugen, sondern die während der Sonnenstunden gewonnene Lichtenergie in einer sinnvollen Form zu speichern und bei Bedarf einzusetzen. Hier ist Wasserstoff ein geeigneter Kandidat.
Architektur im Miniformat – Gerüstbau mit Molekülen
In den Laboren am neuen Center for Nanosystems Chemistry (CNC) und dem nahe gelegenen Fachbereich für Organische Chemie bauen die Forscherinnen daher molekulare Gerüste, die mehrere Ruthenium-Metallzentren näher aneinanderbringe, um deren Leistung so zu verbessern. Eine verlustreiche Aufgabe, wie Mezas Kollegin Schindler beschreibt: „Wir fangen üblicherweise mit etwa fünf Gramm Ausgangstoffen an. Aus denen gewinnen wir nach sieben bis acht Synthesestufen weniger als 100 mg unseres Zielmoleküls.“ Die synthetisierten Gerüste trennen die Forscherinnen dann in über einen Meter hohen Trennsäulen per Größenausschlusschromatographie von den übrigen Molekülbausteinen ab. In den verschieden großen Poren des Packungsmaterials der Trennsäulen werden kleinere Moleküle länger zurückgehalten, während sich Makromoleküle nur in die größeren Poren „verirren“ und daher schneller durch die Säule gelangen. „Dieses Verfahren ist für uns sehr praktisch, da unsere Zielmoleküle so groß sind und deshalb besonders schnell eluieren“, verrät Meza.
Und dann beginnt die eigentliche Arbeit. Zunächst gilt es herauszufinden, ob das hergestellte Gerüst auch tatsächlich mit dem ursprünglichen Bauplan übereinstimmt. Dafür nutzen die Wissenschaftlerinnen das Equipment im gut ausgestatteten Institut. Mit Massenspektrometrie, Kernresonanzspektroskopie und Elementaranalytik gleichen sie die Struktur ihrer Gerüstmoleküle mit den Blaupausen ab. Danach beginnt die Charakterisierung. Hier prüfen die Forscherinnen, was ihr Makromolekül tatsächlich leisten kann. Neben den optischen und elektrischen Eigenschaften, die mittels Spektroskopie und Cyclovoltammetrie untersucht werden, interessieren sie sich vor allem für die Katalysekraft ihrer Produkte. Um diese zu testen, hat das Team in ihrem Labor eine eigene kleine Sonne installiert.
Lesen Sie im Live-im-Labor-Beitrag zum Julius Kühn-Institut, welche Chancen und Risiken Genome Editing für die Pflanzenforschung bereithält:
:quality(80)/images.vogel.de/vogelonline/bdb/1521400/1521464/original.jpg)
Mit molekularem „grünen Daumen“
Live im Labor: Genome Editing als neues Werkzeug der Pflanzenzüchtung
Experimente mit der laboreigenen Mini-Sonne
Den Versuchsaufbau haben die Vorgänger von Meza und Schindler selbst zusammengebaut. Auf einer optischen Bank sind ein Probenbehälter mit Wasserkühlung, optische Linsen und Blenden sowie ein graues Gehäuse mit Lüftungsschlitzen aufgereiht. „Darin ist unsere Xenon-Lampe versteckt, die wir als Lichtquelle nutzen. Die Intensität ihrer Strahlung haben wir so kalibriert, dass sie der Intensität der Sonne entspricht“, erklärt Schindler. In den Probenzylinder füllt die Chemikerin nun einen Mix aus ihrem Gerüstmolekül, das mit Ru2+-Ionen beladenen ist, sowie zwei „Spezialzutaten“. Dann schaltet sie die Mini-Sonne in dem grauen Gehäuse ein. Der Strahl trifft auf die Probe und es passiert – nichts. Zumindest nichts, was man mit dem bloßen Auge sehen könnte. „Die Sauerstoffbildung ist bei unseren kleinen Ansätzen so gering, dass sich erstmal alles gebildete Gas in der Probe löst“, erklärt Schindler.
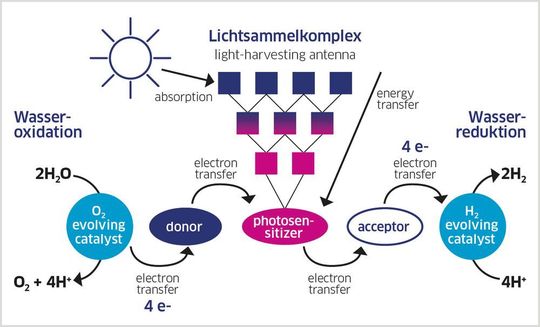
Dass überhaupt Sauerstoff gebildet wird, ist der ersten Spezialzutat im Probenmix zu verdanken: Einem so genannten Photosensibilisator. Er nimmt die einfallende Lichtstrahlung besonders effizient auf und schaltet damit sozusagen den Rutheniumkatalysator ein, indem er das Ru2+ auf höhere Oxidationsstufen oxidiert. „Wir können die anschließende Wasseroxidation dann mithilfe einer Clark-Elektrode verfolgen“, fährt die Doktorandin fort und zeigt auf einen kleinen Einsatz an der Probenküvette. Damit sind minimale Sauerstoffkonzentrationen detektierbar. Auf dem angeschlossenen PC-Bildschirm zeichnet sich eine Sättigungskurve ab, die den gebildeten Sauerstoff darstellt. Darüber gewinnen die Forscherinnen nicht nur Einblicke in die Leistungsfähigkeit ihrer Katalysatoren, sondern können auch Aussagen über die Reaktionskinetik treffen – wichtige Grundlagen für das chemische Verständnis der Reaktion. „Bei der Synthese der Gerüste variieren wir systematisch einzelne Details, z.B. die Größe des Molekülkäfigs, die Anzahl der eingebauten Ruthenium-Zentren oder die Art der Gerüstbausteine“, erzählt Schindler. Mit solchen Testreihen suchen die Chemikerinnen nach Stellschrauben, um die Katalysatorsysteme weiter zu verbessern. Wasserstoff entsteht in ihren Experimenten übrigens keiner. Dafür sorgt die zweite Spezialzutat: Ein Opferreagenz, in diesem Fall Natriumpersulfat. Das nimmt die frei werdenden Elektronen aus der Wasseroxidation auf, die sonst eigentlich für die Wasserstoffgasbildung verwendet würden (s. Abb. 3).
Ein komplexes Puzzle, das Teamwork erfordert

Doch warum hören die Forscherinnen bei der Synthese des Sauerstoffs auf, wo doch Wasserstoff das so heiß begehrte Produkt ist? Die Antwort verrät Joachim Lindner, der als Theoretischer Chemiker seinen Postdoc in der Würthner-Gruppe macht: „Die Systeme, die wir untersuchen, sind aufgrund der eingesetzten Makromoleküle einfach zu komplex.“ Daher hat sich die Arbeitsgruppe auf einen Aspekt spezialisiert. In diesem Fall wollen sie eben die Wasseroxidation besser verstehen – die Teilreaktion, bei der der Sauerstoff entsteht. Lindner modelliert dafür die Gerüste und deren Interaktion mit den Wassermolekülen am PC. So versucht er, die im Laborversuch gemachten Beobachtungen auf molekularer Ebene zu erklären. Dank der Simulationen konnte er z.B. bestätigen, dass ein Gerüst mit drei Ruthenium-Zentren im Ring deshalb besonders effizient ist, weil sich die Wassermoleküle wie Brücken zwischen den Zentren anordnen. Protonen werden so leichter von einem Ort zum anderen innerhalb des Gerüstes weitergegeben. Solche Modelle zu berechnen ist oft zeitintensiv. „Weil die untersuchten Systeme mit den Gerüstmolekülen so groß sind, kann es schon mal zwei Monate dauern, bis man die Ergebnisse einer Modellierung bekommt. Es ist also schon anspruchsvoll, nur Teilprozesse der Photokatalyse zu optimieren. Die einzelnen Teile am Ende in einem gemeinsamen Modell zusammenzubringen wird nochmal schwieriger“, sagt Lindner.
Um das Puzzle zu lösen, arbeitet Würthners Gruppe deshalb mit anderen Teams zusammen, die z.B. die Reduktion untersuchen, bei der das Wasserstoffgas entsteht. Bis die einzelnen Ergebnisse in einem stimmigen Gesamtkonzept vereint werden, wird wohl noch einige Zeit vergehen. Schindler und Meza werden dann vermutlich schon anderer Arbeit außerhalb der Universität nachgehen. Sie zieht es nach Abschluss ihrer Promotion in die Industrie. Und auch wenn ihr Doktorvater Prof. Würthner sehr zufrieden mit der Arbeit der beiden Doktorandinnen ist, freut er sich, wenn seine Schützlinge von der Universitätsforschung in die anwendungsnähere chemische Industrie wechseln. „Unsere oberste Priorität ist ja eigentlich nicht das, was wir wissenschaftlich machen, sondern es sind die Menschen, die wir ausbilden“, betont er. „Hier am Campus betreiben wir klassische Universitätsforschung. Grundlagenforschung zur Photokatalyse. Dahinter steht der Gedanke: Wenn eine Millionen Wissenschaftler weltweit an diesem Thema forschen, dann wird es früher oder später einen Durchbruch geben. Es wäre natürlich schön, wenn gerade wir diejenigen sind, die den Durchbruch schaffen. Aber global gesehen ist es letztlich egal, wer das entscheidende Puzzleteil entdeckt. Die Hauptsache ist, es wird entdeckt.“ Denn eines ist klar: Lange werden die fossilen Rohstoffe unseren Energiehunger nicht mehr stillen können. Die Sonne hat aber noch Milliarden Jahre Strahlkraft, die sie täglich zur Verfügung stellt. Es fehlt nur noch der richtige Dreh, um sie endlich effizient zu nutzen.
Literatur
[1] Aktuelle Fakten zur Photovoltaik in Deutschland (pdf), Fraunhofer ISE, Download von www.pv-fakten.de, Fassung vom 18.3.2019
* C. Lüttmann, Redaktion LABORPRAXIS, E-Mail: Christian.Luettmann@vogel.de
(ID:45904140)







:quality(80)/p7i.vogel.de/wcms/a4/48/a448e4608d93394784d7b364306bc361/0130506959v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/07/29/072962cf54ce048cab6f90214fc58418/image1v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/4a/b6/4ab66927b81ebf966a41081699111fdc/0131598871v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/6c/93/6c93b004f1e78deb7e24da3318766f84/0131138303v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/d7/cd/d7cdb5b2e26d90e0359f008f1e97c4de/0131736983v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/9a/7e/9a7e5bdb654d5b666a01cf46483c8fc7/adobestock-1995567901-editorial-use-only--c2-a9-20stephen-20-e2-80-93-20stock-adobe-com-4000x2251v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/26/d4/26d4f76786d5636186b53e0460f122ad/0131515490v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fa/4b/fa4b5ddaeee6f3883b68b6e2eca825f4/0131696257v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/81/08/8108a3770d79143e5eb43b42fd28766d/0131718320v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/7b/c9/7bc945fec5ec26d7c154890235f42e31/0131662861v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/1b/a2/1ba2d027a8c41332bd5ac2f897250113/0131662713v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/b9/c7/b9c7ab7ddb6e2b3a4f9a2b40541de5f0/0131675956v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/31/9f/319fb620749d359ee20c28483338dc0e/0131664573v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/a0/4d/a04d0563072b334bd4cdc0b5ce498763/0131540240v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/d5/d1d5f369ad43bff37d037f8319c35488/img-5661-jpg-2016x1134v1.webp)
:quality(80)/p7i.vogel.de/wcms/eb/75/eb758271000a58e2b18491419dc13c16/image1v1.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/51400/51447/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/117300/117337/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/60/dd/60ddc39947ebf/brand-logo-registered.png)
:quality(80)/images.vogel.de/vogelonline/bdb/1569200/1569295/original.jpg)
:quality(80)/images.vogel.de/vogelonline/bdb/1569200/1569299/original.jpg)
:quality(80)/images.vogel.de/vogelonline/bdb/1569300/1569300/original.jpg)
:quality(80)/images.vogel.de/vogelonline/bdb/1569300/1569301/original.jpg)
:quality(80)/p7i.vogel.de/wcms/b4/3f/b43f523917bb38e326d4cc02f6622ad7/0130048036v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ed/0d/ed0d186bc89856cc4ba4fa879a0d2ea7/0127495596v2.jpeg)