Long-Covid Langzeitfolgen einer Corona-Erkrankung: mögliche Ursache und Therapie
Eine überstandene Corona-Erkrankung ist nicht in jedem Fall das Ende der Beschwerden. Immer wieder leiden Patienten auch Monate danach noch an Erschöpfung und anderen Symptomen von „Long-Covid“. Eine mögliche Ursache und deren potenzielle Therapie haben nun Forscher aus Lübeck entdeckt.
Anbieter zum Thema
Lübeck – Sie sind müde, schlapp und könne sich schlecht konzentrieren. Schätzungsweise 10 bis 15 % der Corona-Erkrankten leiden auch Wochen bis Monate nach der Infektion noch am so genannten Long-Covid-Syndrom. Damit beschreiben Mediziner diverse Symptome, die nach einer überstandenen Covid-19-Erkrankung beim Betroffenen bleiben.
Bei der Ursachenforschung zu diesen Langzeitfolgen sind Wissenschaftler der Universität zu Lübeck nun einen Schritt weitergekommen. Zusammen mit weiteren Forschern aus Frankreich, Spanien und Deutschland fanden sie heraus, dass SARS-CoV-2 zu einem Gefäßuntergang im Gehirn führt.
Blut-Hirn-Schranke wird angegriffen
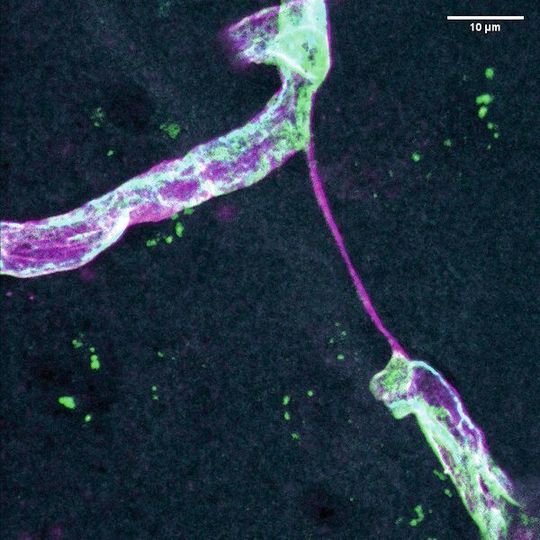
Die Studie unter der Leitung von Markus Schwaninger vom Institut für Experimentelle und Klinische Pharmakologie und Toxikologie der Universität Lübeck zeigt, dass Endothelzellen im Gehirn mit SARS-CoV-2 infiziert werden können, und dass eine solche Infektion zum Zelltod führt. Endothelzellen bilden die innere Schicht aller Gefäße im Körper. Im Gehirn kommt den Endothelzellen eine besonders wichtige Aufgabe zu: Sie bilden eine dichte Schnittstelle zwischen Blut und Gewebe, die so genannte Blut-Hirn-Schranke. Sterben diese Zelle ab, bleibt lediglich die äußere Hülle der Gefäße übrig, die aber nicht mehr von Blut durchströmt werden kann. Dieses Absterben beobachteten die Forscher aus Lübeck in Gehirnproben von verstorbenen Covid-19-Patienten und in Zell- und Tiermodellen einer SARS-CoV-2-Infektion.
Rettet Nemo
Die Wissenschaftler untersuchten die verschiedenen Modelle mit hochentwickelten Techniken wie Einzelzell-RNA-Sequenzierung, Massenspektrometrie und Super-Resolution-Mikroskopie. Dabei fiel ihnen das Enzym Mpro auf, die Hauptprotease SARS-CoV-2. Sie spaltete in den Modellen ein Protein mit der Bezeichnung „Nemo“, welches für das Überleben von Gehirnendothelzellen notwendig ist. Die Spaltung dieses Proteins führt zum Untergang von Blutgefäßen im Gehirn, was Experten als Nekroptose bezeichnen.
:quality(80)/images.vogel.de/vogelonline/bdb/1844000/1844027/original.jpg)
Long-Covid
Corona-Infektion verändert Blutzellen langfristig
Mit ihrer Arbeit bringen die Studienautoren aber auch eine gute Nachricht: Sie wiesen nach, dass die Blockierung der Nekroptose mittels geeigneten Inhibitoren die Durchblutung des Gehirns von Mäusen verbessert. Auf diese Weise könnten Long-Covid-Symptome wie das so genannte Fatigue-Syndrom oder kognitive Beeinträchtigungen, die selbst Kinder und Patienten mit anfänglich leichten Symptomen betreffen, behandelt werden. Die Studie liefert nach Kenntnis der Autoren damit den ersten Beweis für eine direkte Wirkung von SARS-CoV-2 auf die Gefäße des Gehirns und bietet eine neuartige Strategie zur Überwindung neurologischer Folgen von Covid-19.
Originalpublikation: Jan Wenzel, Josephine Lampe, Markus Schwaninger et al.: The SARS-CoV-2 main protease Mpro causes microvascular brain pathology by cleaving NEMO in brain endothelial cells, Nature Neuroscience (2021); DOI: 10.1038/s41593-021-00926-1
(ID:47757640)






:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d8/94/d8946bebf210c5826a6bfd51d610eedc/0130122950v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ce/d1/ced1a66ddc5248ac5c86aa873b3c8d5a/0131387387v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ba/32/ba322cc757f2f82da2839729e0648ca0/0131377715v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/7a/3e/7a3e9478433a525b34c6b34a0aab133f/0131322665v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/14/59/14590acbf17f99545741a47daa2c66e1/5u3a3997-6720x3778v1.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/69/67/696769fab6999/kern-logo2023-blau-4c-or.png)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/27600/27667/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/65/29/6529229873281/gilson-logo-rgb-369x111.png)
:quality(80)/p7i.vogel.de/wcms/ff/a7/ffa76f2f7707c696746e57a0b21800fc/0129222364v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ba/72/ba72ef33a3dd292442d325689955965d/0126695560v2.jpeg)