Titin in Echtzeit verfolgt Riesenprotein im Muskel birgt Überraschungen
Titin ist das größte Protein im Körper und für seine Schlüsselrolle in Muskelgewebe bekannt. Nun ist es Berliner Forschern gelungen, den gesamten Lebenszyklus dieses Riesenproteins in Echtzeit zu verfolgen. So lässt sich beispielsweise untersuchen, wie sich Muskeln nach dem Sport erneuern oder wie sich Herzmuskulatur nach einem Infarkt repariert.
Anbieter zum Thema

Berlin – Während festliche Beleuchtung allerorten die Weihnachtszeit erhellt, freuen sich ForscherInnen am Max-Delbrück-Centrum für Molekulare Medizin (MDC) aus einem ganz anderen Grund über rote und grüne Lichter: Mithilfe fluoreszierender Markierungen hat ein Team den gesamten Lebenszyklus von Titin verfolgt.
Das ist das größte Protein im Körper, das für seine Schlüsselrolle in Muskelgewebe bekannt ist. Titin von seiner Entstehung bis zum Zerfall zu beobachten, habe neuartige Einsichten in die Bildung von Sarkomeren ermöglicht, den kleinsten kontraktilen Einheiten von Herz- und Skelettmuskulatur. Das berichten sie in der Fachzeitschrift Proceedings of the National Academy of Sciences.
Das größte Protein im Körper ist eine Herausforderung
Titin ist ein derart großes Molekül, dass seine Analyse das Team vor einzigartige Herausforderungen gestellt hat. Die WissenschaftlerInnen brachten an entgegengesetzten Enden des Proteins rote und grüne Markierungen an. Das ermöglichte ihnen, die genauen Bewegungen des Titin in aus Mäuseherzen gewonnenen Muskelzellen – den Kardiomyozyten – zu beobachten.
„Kardiomyozyten sind hochspezialisiert und dürfen keinen einzigen Herzschlag lang aussetzen“, sagt Michael Gotthardt, Leiter der Arbeitsgruppe „Neuromuskuläre und kardiovaskuläre Zellbiologie“ am MDC und führender Kopf der Studie. „Wir können jetzt beobachten, wie Titin entsteht und ins Myofilament des Muskels eingefügt wird, während alles andere weiterarbeitet. Das ist ein wunderbarer Anblick.“
Titin ist offenbar weitaus dynamischer als angenommen
Titin in Echtzeit beobachten zu können, ermöglicht neue Erkenntnisse. Seit langem wurde Titin für das starre Rückgrat der Sarkomere gehalten, der kleinsten funktionalen Einheiten von Herz- und Skelettmuskulatur, die sich ausdehnen und zusammenziehen. Es habe sich nun herausgestellt, dass Titin weitaus dynamischer sei als zuvor angenommen, sagt Gotthardt.
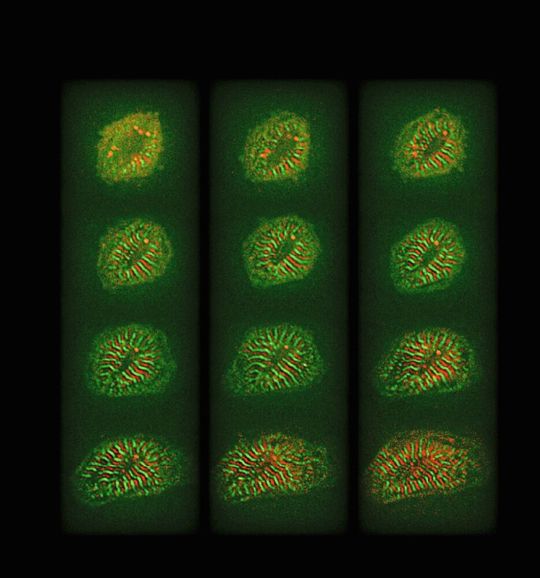
Herzmuskelzellen verfügen anscheinend über einen Vorrat löslichen Titins, der sich durch das Sarkomer verteilt und bereit ist, durch den repetitiven Prozess von Muskelausdehnung und -kontraktion beschädigte Proteine zu ersetzen. Überbeanspruchte Proteine werden aus den Zellen heraustransportiert und abgebaut. Dies alles geschieht innerhalb weniger Stunden, was nach einem schnellen Verlauf klingt, tatsächlich aber sehr viel längere Zeit in Anspruch nimmt als bei jedem anderen Sarkomer-Protein.
Die große Menge Titin außerhalb der Sarkomere war eine Überraschung. Es konnte dank des neuen genetischen Mausmodells und des neuen bildgebenden Verfahrens zum ersten Mal beobachtet werden, berichtet Gotthardt. Ein weiterer unerwarteter Fund war die beobachtete Diversität der Titin-Moleküle, sogenannter Isoformen. Proteine, die sich schneller bewegen, sind wahrscheinlich andere Isoformen als solche, die sich langsamer bewegen.
„Das ist ein Blick auf das wahre Leben der Sarkomere“, sagt Gotthardt. „Wir können so die Bildung und Umgestaltung der Myofilamentstruktur verstehen. Das ist relevant für Erkrankungen und die Entwicklung des Menschen.“
:quality(80)/images.vogel.de/vogelonline/bdb/1541000/1541062/original.jpg)
Studie an größtem Molekül des Menschen
Herzerkrankungen: Protein der Superlative beeinflusst Herzwachstum
Wie erneuern sich Muskeln nach Sport oder der Herzmuskulatur nach einem Infarkt?
Mithilfe der fluoreszierenden Markierungen können WissenschaftlerInnen erforschen, wie sich Muskeln nach dem Sport erneuern oder wie sich Herzmuskulatur nach einem Infarkt repariert. Vielleicht kann man mit ihnen auch Herzerkrankungen besser verstehen, die mit Mutationen in anderen Sarkomer-Proteinen in Zusammenhang stehen, sagt Franziska Rudolph, die Erstautorin der Studie.
„Es ist erstaunlich, endogene Titin-Varianten von Anfang bis Ende in Echtzeit verfolgen zu können“, sagt Rudolph. „Mit diesen Mausmodellen und den unterschiedlichen bildgebenden Verfahren sind viele Experimente möglich.“
Die Technik könnte beispielsweise dafür genutzt werden, implantierte Zellen zu verfolgen – um zu beobachten, wie gut sie sich in das ursprüngliche Muskelgewebe integrieren, ob sie sich einwandfrei mit ihren neuen Nachbarn verbinden, um als Einheit zu arbeiten, oder ob sie das nicht tun. Derartige Erkenntnisse könnten zeigen, ob Zell-Therapien wirksam sind.
Die neuartigen Werkzeuge zu überprüfen und Methoden zur Bildauswertung festzulegen, waren eine Herausforderung, die die Zusammenarbeit mit KollegInnen des Berliner Institut für Medizinische Systembiologie des MDC, der Universitätsmedizin Göttingen und der University of Arizona erforderte. Das Team hat hart daran gearbeitet, zu zeigen, dass die gentechnisch erzeugten fluoreszierenden Proteine keine unerwarteten Nebenwirkungen auf die Entwicklung und Funktion von Muskeln oder Titin hatten.
Mit den neuen Werkzeugen werden die WissenschaftlerInnen weiterhin an Titin forschen. Unter anderem widmen sie sich der Frage, wie Skelettmuskeln auf Sport reagieren.
Originalpublikation: Franziska Rudolph et al. (2019): Resolving titin’s lifecycle and the spatial organization of protein turnover in mouse cardiomyocytes, PNAS, DOI: 10.1073/pnas.1904385116.
* J. Schlütter: Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft, 13125 Berlin
(ID:46290623)







:quality(80)/p7i.vogel.de/wcms/a4/48/a448e4608d93394784d7b364306bc361/0130506959v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/07/29/072962cf54ce048cab6f90214fc58418/image1v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/4a/b6/4ab66927b81ebf966a41081699111fdc/0131598871v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/6c/93/6c93b004f1e78deb7e24da3318766f84/0131138303v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/d7/cd/d7cdb5b2e26d90e0359f008f1e97c4de/0131736983v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/9a/7e/9a7e5bdb654d5b666a01cf46483c8fc7/adobestock-1995567901-editorial-use-only--c2-a9-20stephen-20-e2-80-93-20stock-adobe-com-4000x2251v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/26/d4/26d4f76786d5636186b53e0460f122ad/0131515490v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/01/85/0185e80da045e412b2c5eef7b668c6c5/0131750753v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/fa/4b/fa4b5ddaeee6f3883b68b6e2eca825f4/0131696257v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/81/08/8108a3770d79143e5eb43b42fd28766d/0131718320v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/7b/c9/7bc945fec5ec26d7c154890235f42e31/0131662861v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/b9/c7/b9c7ab7ddb6e2b3a4f9a2b40541de5f0/0131675956v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/31/9f/319fb620749d359ee20c28483338dc0e/0131664573v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/a0/4d/a04d0563072b334bd4cdc0b5ce498763/0131540240v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/d5/d1d5f369ad43bff37d037f8319c35488/img-5661-jpg-2016x1134v1.webp)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/6400/6447/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/68/07/6807ad98568ce/logo-elementar-rgb.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/8800/8870/65.jpg)
:quality(80)/p7i.vogel.de/wcms/a0/11/a011a6500e52a850b377861ff3f07fbb/0125890844v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/91/f7/91f7389c24154676f4edc2da75367a70/0125672504v2.jpeg)