Ferroptose Eisen lässt Zellen sterben
Die Ferroptose bezeichnet eine erst vor kurzem entdeckte Form des Zelltods, die in weiten Teilen noch nicht verstanden ist. Wissenschaftler am Helmholtz Zentrum München stellen nun in zwei Publikationen ein zentrales Enzym vor, welches das tödliche Signal erst möglich macht. Die Erkenntnisse könnten auch in der Forschung zu Krebs und neurodegenerativen Erkrankungen Impulse setzen.
Anbieter zum Thema
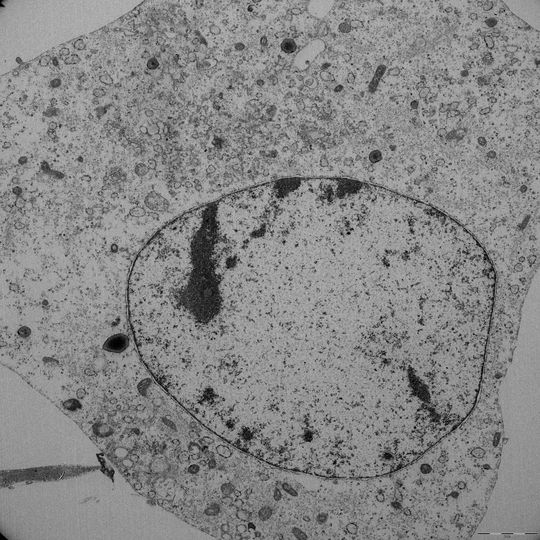
München – Wie der Name schon vermuten lässt, handelt es sich bei der 2012 entdeckten Ferroptose um den organisierten Zerfall von Zellen (griechisch ptosis: der Fall), bei dem zelluläres Eisen eine wichtige Rolle spielt (lateinisch ferrum). „Die einzelnen Mechanismen dieses Zelltodes kristallisieren sich erst langsam heraus und unsere Ergebnisse sind ein wichtiger Beitrag zum Verständnis der Ferroptose“, so Dr. Marcus Conrad, Leiter der Studie und Kopf einer Arbeitsgruppe des Instituts für Entwicklungsgenetik am Helmholtz Zentrum München.
Zusammen mit seinem Team und Kollegen von der Universität Pittsburgh konnte er zeigen, dass das Fettsäurestoffwechsel-Enzym ACSL4 eine zentrale Rolle in der Ferroptose spielt. Denn um den tödlichen Mechanismus auszulösen, muss in der Zelle eine bestimmte Menge an oxidierten Fettmolekülen in der Zellmembran vorliegen. „ACSL4 stellt diese Ausgangsstoffe für das tödliche Lipidsignal bereit und trägt dazu bei, sie in Form von langen ungesättigten Fettsäuren in den Zellmembranen einzulagern“, so Doktorand Sebastian Doll, Erstautor einer der beiden Arbeiten. „Bislang ging man davon aus, dass die Eisen-abhängige Lipidoxidation zufällig auftritt, allerdings zeigen unsere Daten, dass ACSL4 wesentlich zur Entstehung von oxidierten Lipidsignalen bei der Ferroptose beiträgt.“
Anwendung bei Krebs oder neurodegenerativen Erkrankungen denkbar
Obwohl der Begriff Zelltod zunächst einmal nicht gerade gesundheitsförderlich klingt, hat sich speziell in der Krebsforschung gezeigt, dass die kontrollierte Vernichtung von irrläufigen Zellen lebenswichtig für den menschlichen Körper ist. Dementsprechend untersuchten die Wissenschaftler die Rolle von ACSL4 in diesem Zusammenhang: Sie zeigten, dass Zellen, die kein ACSL4 herstellen können, äußerst resistent gegenüber Ferroptose sind und dass solche, die das Enzym exprimieren, sehr empfindlich auf die Auslösung von Ferroptose reagieren. Diese Ergebnisse bestätigten sich auch in weiteren Experimenten an dreifach negativen Brustkrebszellen**. „Das ist insofern interessant, da das Vorhandensein von ACSL4 darüber entscheidet, ob Zellen in Ferroptose gehen können oder nicht“, erklärt Dr. José Pedro Friedmann Angeli, der ebenfalls an beiden Studien beteiligt war. Das Molekül sei daher bei der Stratifizierung von Patienten als Biomarker denkbar.
Und auch einen ersten molekularen Eingriff in die Signalkette konnten die Forscher schon erreichen: Durch Behandlung mit einer Wirkstoffklasse, die eigentlich aus der Diabetestherapie bekannt war (Thiazolidinedione), ließ sich die Ferroptose im Modellversuch verlangsamen.
„Mit unserer neuen Erkenntnis, dass das ACSL4-Enzym wesentlich zu dem Zelltodprozess beiträgt, eröffnen sich völlig neue Therapieansätze zur Hemmung der Ferroptose bei degenerativen Erkrankungen bzw. zu deren Herbeiführung bei bestimmten Tumorerkrankungen“, blickt Studienleiter Conrad voraus. Gerade Tumore, die ansonsten nur schwer mit Standard-Chemotherapeutika zu behandeln seien, könnten sich für eine Ferroptosetherapie eignen, so die Forscher.
Originalpublikationen: Doll, S. et al. (2016): Acsl4 Dictates Ferroptosis Sensitivity by Shaping Cellular Lipid Composition. Nature Chemical Biology, doi: 10.1038/nchembio.2239
Kagan, VE. et al. (2016): Oxidized Arachidonic and Adrenic PEs Navigate Cells to Ferroptosis. Nature Chemical Biology, doi: 10.1038/nchembio.2238
(ID:44380884)







:quality(80)/p7i.vogel.de/wcms/a4/48/a448e4608d93394784d7b364306bc361/0130506959v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/07/29/072962cf54ce048cab6f90214fc58418/image1v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/4a/b6/4ab66927b81ebf966a41081699111fdc/0131598871v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/6c/93/6c93b004f1e78deb7e24da3318766f84/0131138303v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/d7/cd/d7cdb5b2e26d90e0359f008f1e97c4de/0131736983v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/9a/7e/9a7e5bdb654d5b666a01cf46483c8fc7/adobestock-1995567901-editorial-use-only--c2-a9-20stephen-20-e2-80-93-20stock-adobe-com-4000x2251v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/26/d4/26d4f76786d5636186b53e0460f122ad/0131515490v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/01/85/0185e80da045e412b2c5eef7b668c6c5/0131750753v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/fa/4b/fa4b5ddaeee6f3883b68b6e2eca825f4/0131696257v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/81/08/8108a3770d79143e5eb43b42fd28766d/0131718320v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/7b/c9/7bc945fec5ec26d7c154890235f42e31/0131662861v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/b9/c7/b9c7ab7ddb6e2b3a4f9a2b40541de5f0/0131675956v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/31/9f/319fb620749d359ee20c28483338dc0e/0131664573v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/a0/4d/a04d0563072b334bd4cdc0b5ce498763/0131540240v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/d5/d1d5f369ad43bff37d037f8319c35488/img-5661-jpg-2016x1134v1.webp)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/15200/15260/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/69/95/6995807285729/leco-logo-color.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/66/60/666017f181fd3/labv-master-logo.png)
:quality(80)/p7i.vogel.de/wcms/62/b6/62b680afaa71dfaf63111bddb8d64ce4/0126743186v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/06/24/062488fefdd87a6e1e5fae75c917ab12/0128331236v2.jpeg)