Neutronenforschung Optimiertes Hämoglobin von Mensch und Schnabeltier
Jülicher Neutronenforscher konnten zusammen mit französischen und australischen Kollegen zeigen, wie sich das sauerstofftransportierende Protein Hämoglobin an die Körpertemperatur verschiedener Arten anpasst. Wichtige Hinweise gaben dabei Neutronenstreu-Experimente.
Anbieter zum Thema
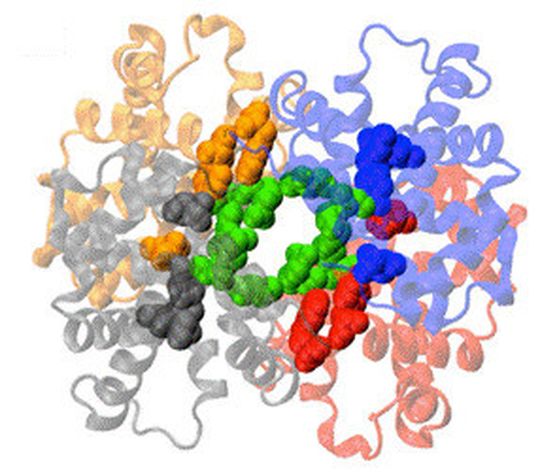
Jülich – Für den gesunden menschlichen Organismus sind etwa 37 °C ideal, Schnabeltiere kommen dagegen schon bei 33 °C gut zurecht. Jülicher Neutronenforscher haben zusammen mit französischen und australischen Kollegen herausgefunden, wie sich das Hämoglobin von verschiedenen Arten im Laufe der Evolution an die unterschiedlichen Körpertemperaturen angepasst hat. Es ist so beschaffen, dass es den Sauerstoff bei der jeweiligen Temperatur optimal von der Lunge in die Zellen transportieren kann.
Dazu haben die Forscher das Hämoglobin mehrerer Arten untersucht, darunter: ein Schnabeltier, das die niedrigste Körpertemperatur der ausgewählten Wirbeltiere aufweist (33 °C), ein Vogel, das gewöhnliche Huhn, mit einer sehr hohen Körpertemperatur von 42,8 °C, sowie ein wechselwarmes Krokodil (25 bis 34 °C). Damit die Sauerstoffmoleküle die vier Eisenatome des Hämoglobins erreichen können, faltet sich das Hämoglobin teilweise auf und wird hinreichend flexibel, ohne dass seine strukturelle Integrität gefährdet wird. Bereits durch frühere Forschungsarbeiten war bekannt, dass die Elastizität der Hämoglobine von verschiedenen Spezies an die unterschiedlichen Körpertemperaturen angepasst ist. Doch welcher temperaturempfindliche Teil des Hämoglobins diese evolutionäre Anpassung bewirkt hat, blieb bisher offen.
Hochsensibles molekulares Thermometer für die Körpertemperatur
Der Schlüssel zu diesem Rätsel sind chemische Unterschiede zwischen den verschiedenen Hämoglobinen. Während sich alle aus Aminosäuren zusammensetzen, variieren die Arten der Aminosäuren und ihre Reihenfolge. Die Forschung konzentrierte sich auf Aminosäuren zwischen kleinen Löchern des Hämoglobins, Höhlen genannt, von denen bekannt ist, dass sie bei der Regulierung der Sauerstoffabsorption eine Rolle spielen. Die Variation dieser Aminosäuren beeinflusst direkt die Steifigkeit des gesamten Proteins und wurde von der Evolution so ausgewählt, dass die Leistungsfähigkeit bei der Körpertemperatur jeder einzelnen Art optimiert wird.
(ID:34529320)






:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d8/94/d8946bebf210c5826a6bfd51d610eedc/0130122950v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ce/d1/ced1a66ddc5248ac5c86aa873b3c8d5a/0131387387v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ba/32/ba322cc757f2f82da2839729e0648ca0/0131377715v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/7a/3e/7a3e9478433a525b34c6b34a0aab133f/0131322665v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/14/59/14590acbf17f99545741a47daa2c66e1/5u3a3997-6720x3778v1.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/115300/115381/65.png)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/6400/6447/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/68/de/68de24cc27215/mp-logo-300dpi-rgb.png)
:quality(80)/p7i.vogel.de/wcms/a6/61/a661fe623c77cad9fd4f85063a2f4d37/0124850082v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/12/ee/12ee90e9d0a90cf8c6131afad80b8292/0126739297v2.jpeg)