Forscher blockieren Transportproteine Türstopper in der Zellmembran
Zellen sind durch eine Membran von ihrer Umgebung abgetrennt. Doch sie können Stoffe gezielt aufnehmen oder abgeben – transportiert über spezielle motorgetriebene Proteine, die wie Drehkreuze Moleküle durch die Membran schleusen. Ein internationales Forscherteam hat nun den Transportmechanismus näher untersucht und herausgefunden, wie sich dieser gezielt unterbinden lässt. Das könnte helfen, Krebszellen daran zu hindern, Chemotherapie-Wirkstoffe aus den Zellen pumpen.
Anbieter zum Thema

Bochum – Zellmembranen grenzen zwar die Zelle von ihrer Umgebung ab, sind aber keineswegs starre, undurchdringbare Barrieren. Viele Stoffe können durch Tunnelproteine durch die Membran hindurch diffundieren oder werden sogar aktiv auf die andere Membranseite befördert. Die Transportproteine, ABC-Exporter genannt, kommen beispielsweise in den Zellmembranen von Bakterien und in großen Mengen in Krebszellen vor und sind dafür verantwortlich, kleine Moleküle aus den Zellen zu befördern. Einige Transporter können Antibiotika oder Chemotherapie-Wirkstoffe aus den Zellen pumpen und die Therapien somit wirkungslos machen.
Mit einem künstlich hergestellten Antikörperfragment hat ein internationales Forschungsteam nun den Transportmechanismus eines ABC-Exporters aus Bakterien untersucht. In der aktuellen Studie arbeiteten die Forscher mit isolierten ABC-Exportern und zeigten, wie die Transportfunktion mit dem Energieantrieb des Proteins zusammenhängt und wie sich beides blockieren lässt.
Für die Studie kooperierten Prof. Dr. Enrica Bordignon und Prof. Dr. Lars Schäfer von der Ruhr-Universität Bochum, beide Mitglied im Exzellenzcluster Ruhr Explores Solvation, mit Prof. Dr. Markus Seeger von der Universität Zürich und Prof. Dr. Mikko Karttunen von der kanadischen University of Western Ontario.
Pforte schließen, und von vorn
Beim Transport von Molekülen aus den Zellen verbrauchen ABC-Exporter Energie. Diese beziehen sie aus der Spaltung des Energiespeichermoleküls ATP auf der Innenseite der Membran. Der ABC-Exporter besteht grob gesagt aus drei Bereichen: dem energieliefernden Motor im Inneren der Zelle; einem Verbindungsstück, das sich durch die Zellmembran erstreckt; und einer Pforte auf der Außenseite der Membran.
:quality(80)/images.vogel.de/vogelonline/bdb/1559200/1559220/original.jpg)
Neue Einblicke in die Zellbewegung
Wie Haie auf Beutesuche: Bewegungsmuster von Zellen
Für den Transportvorgang öffnet sich der ABC-Exporter im Inneren der Zelle, nimmt ein Molekül aus der Zellflüssigkeit auf und transportiert es bis zur anderen Seite der Membran. Dort öffnet sich die äußere Pforte, und das Molekül wird ausgeschieden – aber nur, wenn der Proteinmotor im Inneren ATP spaltet. Erst wenn die äußere Pforte wieder geschlossen ist, kann der nächste Transportvorgang beginnen.
Tür blockiert, Motor aus
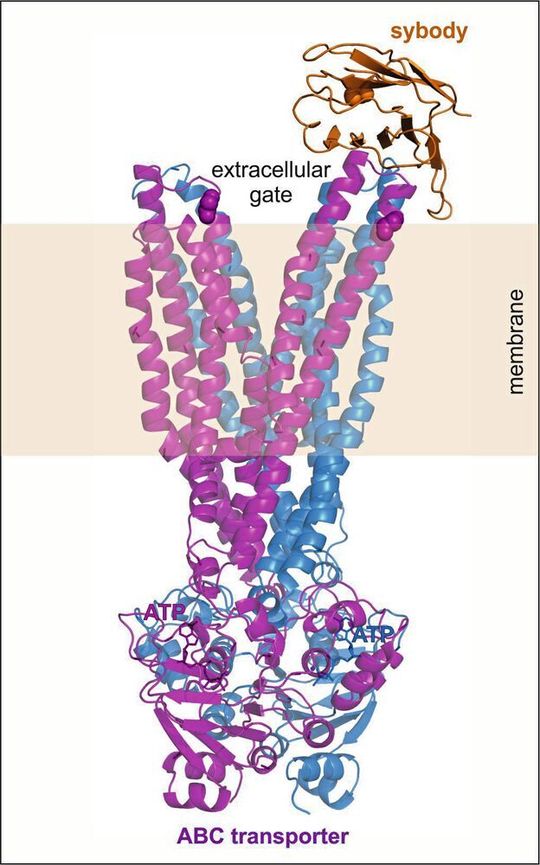
Die Wissenschaftler entwickelten ein künstliches Antikörperfragment, auch Sybody genannt, das im Reagenzglas an den isolierten ABC-Exporter andockt. Mittels Röntgenkristallographie und Elektronenspinresonanz zeigte das Team, dass der Sybody an die geöffnete äußere Pforte bindet. Dadurch konnte sich die Pforte nicht mehr schließen und somit kein neuer Transportvorgang eingeleitet werden. Als Folge davon blieb der Motor im Inneren abgeschaltet; es wurde kein ATP mehr gespalten.
Die Ergebnisse bestätigte die Gruppe in weiteren Experimenten ohne Sybody. In diesen tauschten sie gezielt einige Aminosäuren des Proteins durch genetische Mutation aus; auch das blockierte den Schließmechanismus der äußeren Pforte und die ATP-Spaltung.
„Unsere Analysen haben gezeigt, dass der Mechanismus zum Öffnen und Schließen der äußeren Pforte strukturell mit der Spaltung des Energielieferanten ATP auf der Innenseite zusammenhängt“, beschreibt Bordignon. „Bei unseren Ergebnissen handelt es sich um Grundlagenforschung. Wir hoffen, damit neue Ansätze zur Bekämpfung der Medikamentenresistenz zu eröffnen“, fügt die Leiterin der Bochumer Arbeitsgruppe EPR-Spektroskopie hinzu.
Originalpublikation: Oliver Trapp, Jennifer Teichert, Florian Kruse: Direct Prebiotic Pathway to DNA Nucleosides, Angewandte Chemie, 26 May 2019; DOI: 10.1002/anie.201903400
* Dr. J. Weiler, Ruhr-Universität Bochum, 44801 Bochum
(ID:45981037)







:quality(80)/p7i.vogel.de/wcms/a4/48/a448e4608d93394784d7b364306bc361/0130506959v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/07/29/072962cf54ce048cab6f90214fc58418/image1v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/4a/b6/4ab66927b81ebf966a41081699111fdc/0131598871v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/6c/93/6c93b004f1e78deb7e24da3318766f84/0131138303v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/9a/7e/9a7e5bdb654d5b666a01cf46483c8fc7/adobestock-1995567901-editorial-use-only--c2-a9-20stephen-20-e2-80-93-20stock-adobe-com-4000x2251v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/26/d4/26d4f76786d5636186b53e0460f122ad/0131515490v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/81/08/8108a3770d79143e5eb43b42fd28766d/0131718320v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/7b/c9/7bc945fec5ec26d7c154890235f42e31/0131662861v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/1b/a2/1ba2d027a8c41332bd5ac2f897250113/0131662713v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/c7/92/c792a20f82cca86e2414ee97590b3b29/0131648572v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/b9/c7/b9c7ab7ddb6e2b3a4f9a2b40541de5f0/0131675956v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/31/9f/319fb620749d359ee20c28483338dc0e/0131664573v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/a0/4d/a04d0563072b334bd4cdc0b5ce498763/0131540240v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/d5/d1d5f369ad43bff37d037f8319c35488/img-5661-jpg-2016x1134v1.webp)
:quality(80)/p7i.vogel.de/wcms/2e/17/2e1795b6750cc3eaad6ba81c0bc79d16/0100811496v7.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/69/f8/69f844f48270d/weigert-logo-0126-blau-4c.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/76800/76895/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/62/06/62066242d6e45/kup-logo.jpeg)
:quality(80)/p7i.vogel.de/wcms/77/3c/773caa3fd2d92c51c4c1d838f88b4cfd/0126568559v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/71/7a/717aaa3ac94cbe91abd193385f2d72d2/0126196604v2.jpeg)