Hydrophil oder hydrophob? Benetzung von Oberflächen numerisch untersucht
Die Wechselwirkung von wasserabweisenden und wasserfreundlichen Molekülen wird in vielen industriellen Prozessen ausgenutzt. Doch woher kommen diese Effekte? Lesen Sie in diesem Beitrag, wie dies mithilfe quantenmechanischer Simulationen untersucht werden kann.
Anbieter zum Thema
Das Benetzungsverhalten von Oberflächen ist von fundamentaler Bedeutung für technologische Anwendungen und in vielen Naturwissenschaften. Beispielsweise werden Struktur und Funktion von Proteinen stark von der molekularen Wechselwirkung mit der wässrigen Umgebung bestimmt oder die Benetzung von Motorteilen mit Öl ist entscheidend für das Verschleiß- und Reibverhalten. Ein weiteres bekanntes Beispiel ist der Lotoseffekt, die Selbstreinigung von Lotospflanzen, aber auch vieler weiterer Pflanzen durch wasserabweisende (hydrophobe) Oberflächen auf denen Wassertropfen leicht abperlen und dabei Schmutzpartikel aufnehmen und entfernen. Als hydrophil (wasserliebend) werden Oberflächen bezeichnet, die sehr gut von Wasser benetzt werden. Hydrophile Materialien kommen z.B. zur Effiziensteigerung von Kühlsystemen zum Einsatz.
Polare Hydrophobie
Auf mikroskopischer Ebene werden polare Moleküle bzw. Oberflächen allgemein mit hydrophil gleichgesetzt, während apolar mit hydrophob gleichgesetzt wird. Grund hierfür ist die Annahme einer starken elektrostatischen Wechselwirkung zwischen polaren Materialien und den ebenfalls polaren Wassermolekülen bzw. das Fehlen einer elektrostatischen Wechselwirkung im Fall apolarer Oberflächen. Von der Regel polar=hydrophil und apo-lar=hydrophob gibt es jedoch eine wichtige Ausnahme, die Klasse der perfluorierten Kohlenstoffmaterialien (s. LP-Tipp).
Die numerische Methode
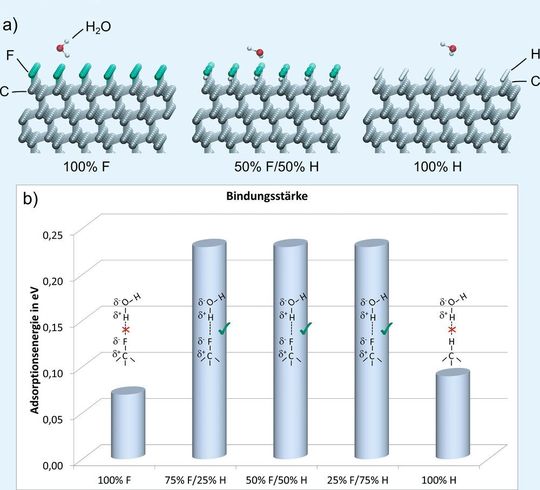
Um der molekularen Ursache der polaren Hydrophobie auf die Spur zu kommen, wurde von Fraunhofer-Wissenschaftlern eine Multiskalensimulationsmethode entwickelt, die eine Vorhersage der Benetzung von Oberflächen erlaubt. Ausgehend von einer quantenmechanischen Beschreibung der Valenzelektronen im Rahmen der Dichtefunktionaltheorie (DFT) wird dabei zunächst die Wechselwirkung einzelner Flüssigkeitsmoleküle mit einer bestimmten Oberfläche berechnet. Die dabei gewonnenen Ergebnisse fließen anschließend in das Modell eines klassischen Kraftfelds ein, welches das Verhalten ausgedehnter Tröpfchen auf der Oberfläche beschreibt. Als Modellsystem zur Untersuchung der polaren Hydrophobie wurden zunächst fluorierte Diamantoberflächen untersucht (s. Abb. 1a). Anschließend wurden die dabei gewonnenen Ergebnisse auch für molekulare perfluorierte Kohlenstoffe bestätigt.
Die DFT-Rechnungen bestätigten zum einen den stark polaren Charakter der zu 100% mit Fluoratomen terminierten Diamantoberfläche und zum anderen die relativ schwache Anbindung (Hydrophobie) einzelner Wassermoleküle. Um den Effekt der Fluorierung besser zu verstehen, wurden nun sukzessive die Fluoratome durch Wasserstoffatome ersetzt bis eine zu 100% mit Wasserstoffatomen terminierte Oberfläche erzeugt wurde. Dabei zeigte sich erstaunlicherweise eine stark erhöhte Anbindungsstärke von Wassermolekülen auf den Oberflächen, welche sowohl mit Wasserstoffatomen als auch Fluoratomen abgesättigt waren. Hingegen war die Neigung von Wassermolekülen, sich an die apolare mit 100% Wasserstoffatomen bedeckte Oberfläche zu binden, erwartungsgemäß wiederum nur schwach ausgeprägt (s. Abb. 1b).
Doch warum können Fluoratome in C-F-Bindungen in manchen Situationen gute Akzeptoren für Wasserstoffbrückenbindungen sein (gemischte Wasserstoff/Fluor-Terminierung), während sie in anderen Situationen schlechte Akzeptoren sind (reine Fluor-Terminierung)? Wie die Simulationen zeigten, liegt es nicht an den einzelnen C-F-Bindungen selbst, welche in beiden Fällen ganz ähnliche Eigenschaften besitzen. Einen Hinweis ergibt jedoch die Analyse des oberflächennahen elektrischen Feldes: Eine vollständige Terminierung mit Fluoratomen und somit dichtgepackte C-F-Dipole auf der Oberfläche führen zu einem sehr schnell abfallenden elektrischen Feld, sodass Wassermoleküle nicht in den Bereich hoher Feldstärken vordringen können und somit auch elektrostatisch mit der Diamantoberfläche nicht wechselwirken. Hingegen weist die gemischte Wasserstoff-/Fluorterminierung mit einer gerningeren Dichte an C-F-Dipolen auch noch in einiger Entfernung von der Oberfläche ein beträchtliches elektrisches Feld auf, welches die Wassermoleküle anzieht und somit stärker anbindet (s. Abb. 2). Interessanterweise wurde dieser schnelle Abfall des elektrischen Feldes bereits 1928 von Lennard-Jones für dichte Gitter aus mathematischen Dipolen vorhergesagt, aber bisher nicht mit der polaren Hydrophobie in Verbindung gebracht.
(ID:44158918)






:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d8/94/d8946bebf210c5826a6bfd51d610eedc/0130122950v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ce/d1/ced1a66ddc5248ac5c86aa873b3c8d5a/0131387387v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ba/32/ba322cc757f2f82da2839729e0648ca0/0131377715v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/7a/3e/7a3e9478433a525b34c6b34a0aab133f/0131322665v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/14/59/14590acbf17f99545741a47daa2c66e1/5u3a3997-6720x3778v1.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/131900/131910/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/67/c9/67c9a358ae891/asecos-box-rot-4c-250x250px.png)
:fill(fff,0)/p7i.vogel.de/companies/69/2e/692ed0d59df43/a1sciences-4c-transparenter-hintergrund.png)
:quality(80)/images.vogel.de/vogelonline/bdb/1059800/1059869/original.jpg)
:quality(80)/images.vogel.de/vogelonline/bdb/1059800/1059872/original.jpg)
:quality(80)/images.vogel.de/vogelonline/bdb/1059800/1059871/original.jpg)
:quality(80)/images.vogel.de/vogelonline/bdb/1059800/1059870/original.jpg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0131240119v5.jpeg)
:quality(80)/p7i.vogel.de/wcms/f5/ea/f5ea9b22a7e3774b8ca8a19e9db95915/0131239927v10.jpeg)