Funktionale Proteinkomplexe Hohe räumliche und zeitliche Auflösung – Neuer Ansatz zur Analyse komplexer Proteininteraktionen
Heidelberger Wissenschaftlern ist es gelungen, eine lange bestehende Hürde in der molekularen Zellbiologie zu überwinden: Ihre neu entwickelte Technik kombiniert zwei bestehende Ansätze und erlaubt auf diese Weise die einfache Analyse kontextabhängiger Proteinkomplexe mit bislang unerreichter räumlicher und zeitlicher Auflösung. Die Forscher erhoffen sich davon ein besseres Verständnis der dynamischen Reaktionen von Zellen mit ihrer Umgebung.
Anbieter zum Thema
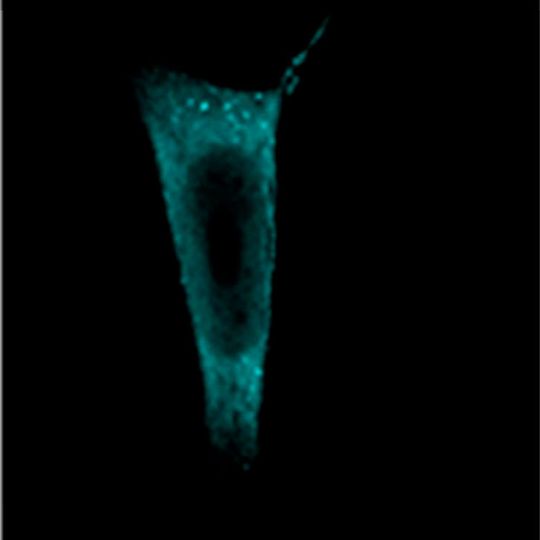
Heidelberg – Die Zusammensetzung bestimmter funktionaler Proteinkomplexe kann künftig mit beispielloser Auflösung in ihrer Zellumgebung analysiert werden. Möglich wird dies durch eine neue Untersuchungsmethode, die das Team von Nachwuchsgruppenleiter Dr. Julien Béthune am Biochemie-Zentrum der Universität Heidelberg entwickelt hat.
Damit ist es den Wissenschaftlern gelungen, eine lange bestehende Hürde in der molekularen Zellbiologie zu überwinden. Zum Einsatz kommen soll die neue Technik mit dem Namen „split-BioID“ nun bei sogenannten kontextabhängigen Proteinkomplexen, die mit den bisherigen Verfahren nicht analysiert werden konnten.
Überprüfung funktionaler Proteinkomplexe
Das Genom lebender Organismen kodiert zehntausende von Proteinen, die eine Vielzahl von Funktionen in der Zelle übernehmen. Damit sie diese Aufgaben erfüllen können, müssen die Proteine mit einander interagieren und sich zu größeren makromolekularen Komplexen zusammenschließen. Für die molekulare Zellbiologie ist die Identifikation von Proteininteraktionen innerhalb solcher Komplexe ein bedeutendes Forschungsfeld.
Eine Herausforderung für die Analyse stellt allerdings ihre dynamische Struktur dar. „In der Regel gehört ein einzelnes Protein zu mehreren unterschiedlichen und oftmals überlappenden Komplexen, die sich wiederum je nach Zellkontext und Funktion in der Zelle ändern“, erläutert Dr. Bethune. „Bislang scheiterte die leichte Zuweisung von Proteininteraktionen zu größeren Komplexen an der fehlenden Auflösung.“
Besseres Verständnis dynamischer Reaktionen von Zellen mit ihrer Umgebung
In ihrer Forschung kombinieren die Wissenschaftler zwei bereits bestehende Ansätze: Zum einen wird ein Nachweisverfahren namens BioID eingesetzt, das mögliche Interaktionen eines Proteins mithilfe von Markierungen identifiziert. Ergänzt wird dieses Verfahren durch das Konzept des „Protein-Fragments Complementation Assay“ (PCA), einer Methode zum Nachweis von Interaktionen zwischen zwei Proteinen.
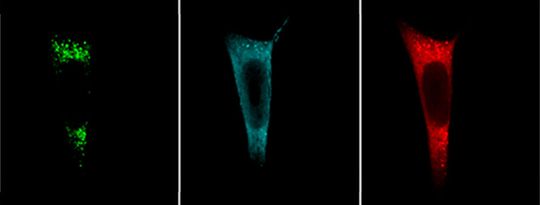
„Im Vergleich zu den konventionellen Methoden bietet das neue ,split-BioID‘ eine herausragende räumliche und zeitliche Auflösung und ermöglicht die einfache Analyse kontextabhängiger Proteinkomplexe“, betont Isabel Schopp, Doktorandin in der Arbeitsgruppe von Dr. Béthune und Erstautorin der Studie. Die Wissenschaftler erhoffen sich nun ein besseres Verständnis der dynamischen Reaktionen von Zellen mit ihrer Umgebung.
Im Rahmen des Exzellenzclusters CellNetworks der Universität Heidelberg forscht Julien Béthune am Biochemie-Zentrum zu den Mechanismen der posttranskiptionellen Genabschaltung durch die microRNA und ihrem Zusammenspiel mit der Endomembran.
Originalpublikation: I.M. Schopp, C.C.A. Ramirez, J. Debeljak, E. Kreibich, M. Skribbe, K. Wild, and Julien Béthune: Split-BioID a conditional proteomics approach to monitor the composition of spatiotemporally defined protein complexes. Nature Communications 8:15690 (published online 6 June 2017), doi: 10.1038/ncomms15690
(ID:44735067)







:quality(80)/p7i.vogel.de/wcms/63/2b/632b7c3001c517c32711dac6298f8707/0131501813v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/26/d4/26d4f76786d5636186b53e0460f122ad/0131515490v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/39/fe/39fe2cd50f7947927c078ad83987abf2/microbiome-04-jpg-2cqtransformid-3d15081-2casite-3ddefaultde-pagespeed-ce--ofz-tqfod-750x422v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/cd/e5/cde57faefc6531041e587a2fde0220ef/image1-1322x744v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/13/8f/138f41de403c0c81139657dae230188d/0131503024v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a0/4d/a04d0563072b334bd4cdc0b5ce498763/0131540240v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/d5/d1d5f369ad43bff37d037f8319c35488/img-5661-jpg-2016x1134v1.webp)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/57/11/5711ba14776b6e702c9e775a14837239/0131582930v2.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/66/71/66716b11ad4e1/gerstel-logo-mlw.png)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/6400/6447/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/62/06/62066242d6e45/kup-logo.jpeg)
:quality(80)/p7i.vogel.de/wcms/e7/8d/e78d3dcdafc0bb38efe8e107a8de14be/0130009974v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/13/6e/136e0248969909506e20df82ef37044e/0127415831v1.jpeg)