Computersimulation Wie bewegt sich der Erreger der Schlafkrankheit?
Verbesserte Kontrollen haben laut WHO dazu geführt, dass die Zahl der gemeldeten Infektionen mit der Schlafkrankheit in Afrika in den vergangenen Jahren rückläufig gewesen ist. Trotzdem geht von der oftmals tödlichen Krankheit immer noch eine Gefahr aus. Mithilfe eines Computer-Modells konnten Physiker der TU Berlin die Fortbewegung des Erregers der Schlafkrankheit analysieren. Diese Erkentnisse können in Zukunft zu besseren Therapien führen.
Anbieter zum Thema
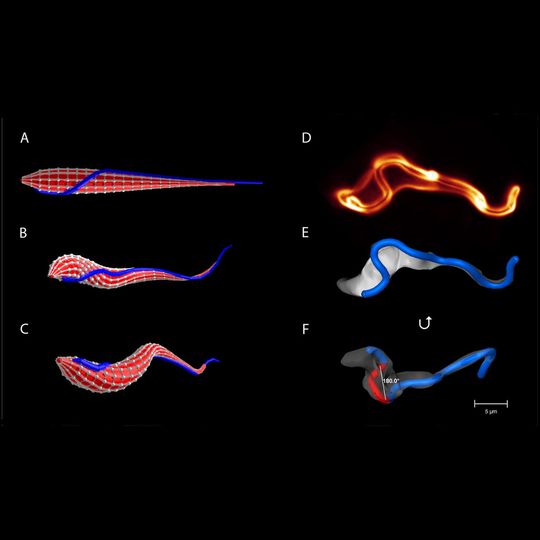
Berlin; Würzburg – Trypanosoma brucei heißt der unscheinbare einzellige Organismus, der die Schlafkrankheit auslöst – eine sowohl für Menschen wie für Tiere potenziell tödliche Krankheit. Übertragen wird der Erreger von der Tsetse-Fliege. Im Blutkreislauf seiner Wirte vermehrt er sich massiv und kann dann – beim nächsten Biss der Fliege – wieder aufgenommen und weiter verbreitet werden. Innerhalb der Fliege durchläuft der Erreger verschiedene morphologische Formen.
Im Laufe seines Lebens muss sich der Einzeller in den verschiedensten Umgebungen zurechtfinden: Im Blutkreislauf der Säugetiere sowie in den Verdauungsorganen und in den Speicheldrüsen der Fliege. Fortbewegen kann er sich in allen Fällen mithilfe eines außen an den spindelförmigen Zellkörper angehängten Flagellums (Fadens) durch dessen Schlag eine so genannte „interne Biegewelle“ ausgelöst wird.
Videoaufnahmen zur Erstellung eines Computermodells
„Dass das Trypanosom mithilfe des Flagellums schwimmt, war klar“, so Prof. Dr. Holger Stark, Leiter der Arbeitsgruppe Statistische Physik weicher Materie und biologischer Systeme am Institut für Theoretische Physik der TU Berlin, „unklar war aber, wie genau das Schwimmen funktioniert.“ Diesem Mechanismus sind Holger Stark und seine Mitarbeiter zusammen mit Kollegen der Abteilung für Zell- und Entwicklungsbiologie der Universität Würzburg auf die Schliche gekommen.
„Dazu haben wir anhand von detaillierten Videoaufnahmen, die unter dem Mikroskop der Würzburger Kollegen entstanden sind, ein so genanntes In-silico-Modell (Computer-Modell) erstellt und es in zahlreichen Versuchsreihen so nahe wie möglich an die Realität angeglichen. Dabei besteht die größte Schwierigkeit bei solchen numerischen Modellen darin, den Zellkörper so zu modulieren, dass er auch während der Schwimmbewegungen stabil bleibt“, weiß Holger Stark.
Nachdem dieser Schritt gelungen war, konnte der Mitarbeiter von Holger Stark, Dr. Davod Alizadehrad, an dem Modell Experimente simulieren, die in einem biologischen Versuch ungleich aufwändiger oder gar unmöglich gewesen wären. „Zum Beispiel haben wir verschiedene Anheftungspunkte für das Flagellum und deren Auswirkungen auf das Schwimmverhalten in Wasser getestet. In dem Original ist das Flagellum in einer halben Spirale um den Zellkörper angeheftet. In dem In-silico-Modell haben wir diese Spirale vergrößert oder verkleinert und konnten zeigen, dass jede Veränderung gegenüber der Original-Anheftung des Flagellums die Schwimmgeschwindigkeit des Trypanosoms deutlich herabsetzt. Die Evolution hat da also die optimale Struktur gefunden.“
Warum schwimmen Trypanosome in Blut schneller als in Wasser?
In den nächsten Schritten soll untersucht werden, wie sich die Form des Trypanosoms und seine Schwimmbewegung, abhängig von den verschiedenen Flüssigkeiten, in denen es sich bewegt, verändern. „Trypanosomen schwimmen zum Beispiel in elastisch-viskosen Flüssigkeiten wie Blut schneller als in Wasser. Indem wir in unseren Simulationen Hindernisse wie die roten Blutkörperchen aufnehmen, können wir genau studieren, wie das möglich ist. Auch die Entwicklung des Trypanosoms innerhalb der Tsetse-Fliege ist bislang weniger charakterisiert. Hier kann das In-silico-Modell wertvolle Unterstützung leisten, indem es simuliert, wie die morphologischen Veränderungen die Fortbewegung oder auch die Interaktion des Erregers mit seiner Umgebung beeinflussen“, so Holger Stark zu der Zukunft des Projektes. „Erste Schritte dazu sind getan.“
Originalpublikation:
PLoS Comput. Biol. 11, e1003967 (2015): Davod Alizadehrad, Timothy Krüger, Markus Engstler, Holger Stark, Simulating the Complex Cell Design of Trypanosoma brucei and Its Motility
(ID:43161275)







:quality(80)/p7i.vogel.de/wcms/63/2b/632b7c3001c517c32711dac6298f8707/0131501813v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/26/d4/26d4f76786d5636186b53e0460f122ad/0131515490v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/39/fe/39fe2cd50f7947927c078ad83987abf2/microbiome-04-jpg-2cqtransformid-3d15081-2casite-3ddefaultde-pagespeed-ce--ofz-tqfod-750x422v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/cd/e5/cde57faefc6531041e587a2fde0220ef/image1-1322x744v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/13/8f/138f41de403c0c81139657dae230188d/0131503024v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a0/4d/a04d0563072b334bd4cdc0b5ce498763/0131540240v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/d5/d1d5f369ad43bff37d037f8319c35488/img-5661-jpg-2016x1134v1.webp)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/57/11/5711ba14776b6e702c9e775a14837239/0131582930v2.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/40400/40477/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/67/e2/67e2c251f40d9/zefa-group-logo---1-.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/67/c9/67c9a358ae891/asecos-box-rot-4c-250x250px.png)
:quality(80)/p7i.vogel.de/wcms/7b/5b/7b5be8ee0f1701f64f09e040820c654a/0128080826v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/de/19/de199c3204d1e68b0f98f5da76d0999e/0125905629v2.jpeg)