HIV Wo sich Aids-Viren in Zellen verstecken
HI-Viren bevorzugen Plätze gleich hinter der Eintrittspforte zum Zellkern – ein Forscherteam des Universitätsklinikums Heidelberg und des Deutschen Zentrums für Infektionsforschung entdeckte, warum das genetische Material von HI-Viren an bestimmten Stellen des menschlichen Erbguts besonders häufig integriert wird.
Anbieter zum Thema
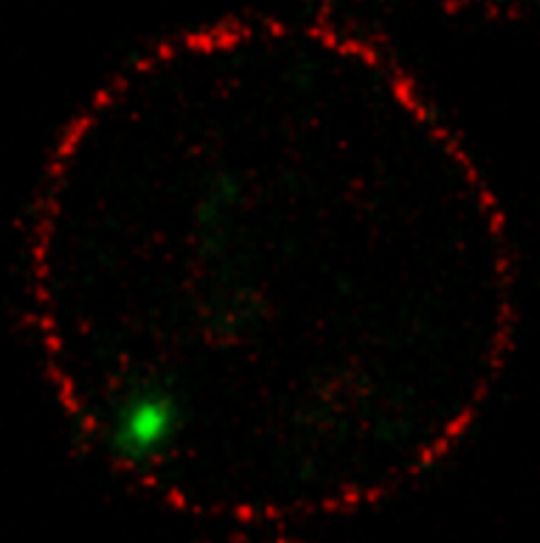
Heidelberg – Haben Aids-Viren eine Zelle des menschlichen Immunsystems infiziert, lassen sie ihr genetisches Material im Zellkern in die menschliche Erbinformation (DNS) einbauen. Weiter als in den Eingangsbereich des Zellkerns kommen sie dabei meistens nicht, wie Wissenschaftler des Zentrums für Infektiologie (Zentrumssprecher: Professor Dr. Hans-Georg Kräusslich) am Universitätsklinikum Heidelberg und des Deutschen Zentrums für Infektionsforschung (DZIF) in Zellversuchen nun entdeckten: Die Erbinformation der HI-Viren findet sich besonders häufig in den aktiven DNS-Abschnitten direkt hinter den Eintrittspforten zum Zellkern, den Kernporen. „Man kann sich das in etwa vorstellen wie bei einem verspäteten Besucher einer Veranstaltung. Er kommt durch die Tür und nimmt den erstbesten freien Sitzplatz“, beschreibt Dr. Marina Lusic, Leiterin einer Arbeitsgruppe des Bereichs Virologie.
Die renommierte Virologin Dr. Marina Lusic wechselte 2014 vom Molecular Medicine Laboratory in Triest, Italien, nach Heidelberg, um im Rahmen des Deutschen Zentrums für Infektionsforschung (DZIF) in enger Zusammenarbeit mit führenden Forschungsgruppen aus ganz Deutschland die Funktionsweise des HI-Virus weiter zu entschlüsseln.
Versteckspiel der Viren macht HIV bis heute unheilbar
Die aktuell veröffentlichten Ergebnisse sind ein erster Schritt zum besseren Verständnis, wie HI-Viren ihre Erbinformation in der Zelle verstecken. Verborgen im Zellkern im menschlichen Erbgut und vorübergehend deaktiviert ist sie weder erreichbar für die Abwehrmechanismen der Zellen noch für Medikamente, die nur freie Viren im Blut vernichten können. Virologen bezeichnen dieses Versteckspiel als Latenz. Sie ist der Grund, warum HIV bis heute nicht heilbar ist: Sobald die Medikamente abgesetzt werden, wird die schlummernde Erbinformation der Viren wieder aktiv und führt damit zur Produktion und Vermehrung neuer Viren, die dann den Körper überschwemmen. „Erst, wenn wir die Mechanismen der HIV-Latenz kennen, werden wir in der Lage sein, therapeutische Gegenmaßnahmen zu entwickeln“, so Lusic.
Bereits zuvor war bekannt, dass HI-Viren ihr Erbmaterial nicht wahllos in das menschliche Genom integrieren. Sie nutzen bevorzugt eine Reihe häufig aktiver DNS-Abschnitte (Gene), die an unterschiedlichen Zellfunktionen beteiligt sind. Wie es zu dieser Auswahl unter den rund 20.000 Genen des menschlichen Genoms kommt, konnte man sich bisher allerdings nicht erklären. Des Rätsels Lösung klingt banal: Alle diese Gene befinden sich in unmittelbarer Nähe der Kernporen. An infizierten Zellen unter dem Mikroskop zeigte sich: Das farblich markierte Genmaterial der HI-Viren wird in die nächsten aktiven Gene eingebaut, auf die es nach dem Eintritt durch die Kernporen stößt. In eben diesen Bereichen rund um die Kernporen befinden sich in der Regel genau die Gene, die zuvor bereits – ohne den Zusammenhang zu kennen – als bevorzugtes Ziel der Viren identifiziert worden waren. In den weiter mittig gelegenen Bereichen des Zellkerns fand sich dagegen kaum genetisches Material der Viren.
HIV benötigt Bausteine der Kernporen für weitere Entwicklungsschritte
Um sich in das menschliche Erbgut einbauen zu können, benötigen die HI-Viren die Hilfe bestimmter zelleigener Proteine. „Eine wichtige Rolle spielten dabei Eiweißbestandteile der Kernporen. Das ist wahrscheinlich ein Grund dafür, warum HIV in den Bereichen unmittelbar hinter den Kernporen bleibt“, erklärt Dr. Lusic. Ist HIV erst einmal in die Erbinformation eingefügt, kann es die Zelle dazu umprogrammieren, ab sofort nur noch Kopien des Virus in großer Menge herzustellen und sich damit schließlich selbst zu zerstören. Oder es bleibt zunächst inaktiv und wartet ab. Warum sich ein Teil der Viren erst einmal für unbestimmte Zeit selbst deaktivieren, ist bisher noch völlig unklar. Dieser Frage möchte Dr. Marina Lusic mit ihrem Team als nächstes nachgehen.
Im Deutschen Zentrum für Infektionsforschung (DZIF) entwickeln bundesweit mehr als 150 Wissenschaftler aus 32 Institutionen gemeinsam neue Ansätze zur Vorbeugung, Diagnose und Behandlung von Infektionskrankheiten. Ziel ist die sogenannte Translation, die schnelle, effektive Umsetzung von Forschungsergebnissen in die klinische Praxis. Damit bereitet das DZIF den Weg für die Entwicklung neuer Impfstoffe, Diagnostika und Medikamente gegen Infektionen.
Originalpublikation: Bruna Marini, Attila Kertesz-Farkas, Hashim Ali, Bojana Lucic, Kamil Lisek, Lara Manganaro, Sandor Pongor, Roberto Luzzati, Alessandra Recchia, Fulvio Mavilio, Mauro Giacca & Marina Lusic. Nuclear architecture dictates HIV-1 integration site selection. Nature (2015) doi: 10.1038/nature14226
* J. Bird: Universitätsklinikum Heidelberg, 69120 Heidelberg
(ID:43307204)






:quality(80)/p7i.vogel.de/wcms/63/2b/632b7c3001c517c32711dac6298f8707/0131501813v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/26/d4/26d4f76786d5636186b53e0460f122ad/0131515490v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/39/fe/39fe2cd50f7947927c078ad83987abf2/microbiome-04-jpg-2cqtransformid-3d15081-2casite-3ddefaultde-pagespeed-ce--ofz-tqfod-750x422v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/cd/e5/cde57faefc6531041e587a2fde0220ef/image1-1322x744v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/13/8f/138f41de403c0c81139657dae230188d/0131503024v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a0/4d/a04d0563072b334bd4cdc0b5ce498763/0131540240v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/d5/d1d5f369ad43bff37d037f8319c35488/img-5661-jpg-2016x1134v1.webp)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/115900/115965/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/69/f8/69f844f48270d/weigert-logo-0126-blau-4c.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/62/06/62066242d6e45/kup-logo.jpeg)
:quality(80)/p7i.vogel.de/wcms/4c/b1/4cb1f4fc5bfabbb1caa2e653d83c250f/0124642099v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/9a/2c/9a2c29461a7363766921da706c18915a/0129780133v2.jpeg)