Sequenzierung einzelner Proteine Zellpore als Scanner für Aminosäuren
Aminosäuren sind wie Perlen auf einer Kette zu Proteinen gereiht. Eine direkte Analyse dieser Perlenabfolge war bislang jedoch nicht möglich. Nun hat ein internationales Forscherteam eine Methode entwickelt, die als Grundlage für eine direkte Sequenzierung einzelner Proteine fungiert.
Anbieter zum Thema
Freiburg – In Zellen arbeiten Proteine rund um die Uhr, um die biologischen Funktionen des Körpers aufrechtzuerhalten. Sie helfen als Enzyme bei chemischen Reaktionen, dienen als Transporter oder Kanal für Nähr- und Botenstoffe, sind Stützpfeiler oder Signalgeber. Jedes Protein ist eine dreidimensional gefaltete Kette aus unterschiedlichen Aminosäuren, deren Abfolge genetisch festgelegt ist.
Während Forscher die Sequenz eines einzelnen DNA-Stranges bereits auslesen können, war eine solche direkte Analyse für die Aminosäurresequenz einzelner Proteine bisher noch nicht möglich. Ein Team aus Forschern der französischen Universität Cergy-Pontoise, der Universität Freiburg und der amerikanischen Universität von Illinois hat nun erstmals eine solche Analyse geschafft. Mithilfe einer winzigen Pore von Nanometergröße identifizierten sie einzelne Aminosäuren in kurzen Peptiden, also Bruchstücken von Proteinen. Damit haben die Wissenschaftler die Grundlagen für eine direkte Sequenzierung einzelner Proteine gelegt.
Stau in der Pore verrät Molekülgröße
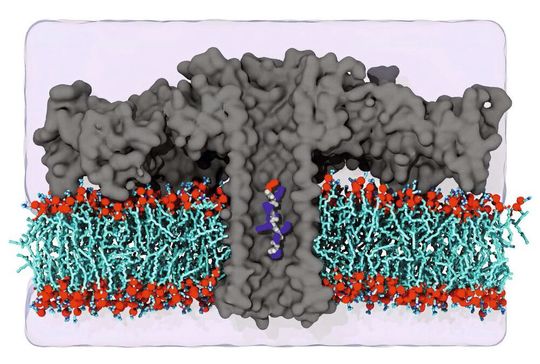
Bisherige Techniken wie die Massenspektrometrie sind nicht empfindlich genug, um zum Beispiel die Proteinzusammensetzung einer einzelnen Zelle fehlerfrei zu bestimmen. Deshalb haben die Forscher um Prof. Dr. Jan C. Behrends von der Universität Freiburg eine alternative Methode entwickelt. Sie bauten das porenbildende Protein Aerolysin in eine künstliche Zellmembran ein und ließen dann durch die Pore einen Ionenstrom fließen.
Wie vorige Ergebnisse gezeigt hatten, lässt sich dieser Ionenstrom sehr präzise Messen. Wird er von einem in die Pore eintretenden Molekül verringert, kann man auf die Größe dieses Moleküls schließen. Wie das Team nun zeigte, ist die Empfindlichkeit der so genannten Aerolysinpore so groß, dass man damit Peptide voneinander unterschieden kann, wenn sie nur in einer Position unterschiedliche Aminosäuren aufweisen.
:quality(80)/images.vogel.de/vogelonline/bdb/1602100/1602106/original.jpg)
Kontoverse um Kaliumkanäle gelöst
Kommt Kalium „trocken“ durch die Zellmembran?
Gleich schwer, aber trotzdem unterscheidbar
Mit einer besonders hochauflösenden, elektrophysiologischen Messmethode gelang es sogar, die Aminosäuren Leucin und Isoleucin mit mehr als 90 Prozent Zuverlässigkeit zu unterscheiden. Diese beiden Aminosäuren besitzen die gleiche Zusammensetzung, also Masse, und weisen lediglich eine unterschiedliche räumliche Anordnung der Molekülgruppen auf. Die Unterscheidung solcher Strukturisomere mithilfe der Aerolysin-Pore beweist, dass das Stromsignal nicht ausschließlich von der Molekülmasse abhängt.
Weiterhin bedeutet dies, dass die neue Technologie der Massenspektrometrie prinzipiell überlegen ist. Die Forscher in den USA zeigten in Simulationen, dass die hohe Auflösung auf einer Art molekularer Falle innerhalb der Pore basiert. Diese Falle stellt die Peptide für ungefähr eine Hundertstelsekunde ruhig, was die genaue Messung erst ermöglicht. Dadurch konnten für die jetzt veröffentlichte Studie 11 der 20 am Aufbau von Proteinen beteiligten Aminosäuren mithilfe des Nanoporen-Stromsignals ohne zusätzliche chemische Veränderung zuverlässig unterschieden werden.
Originalpublikation: Ouldali, H., Sarthak, K., Ensslen, T., Piguet, F., Manivet, P., Pelta, J., Behrends, J.C., Aksimentiev, A., Oukhaled, A.: Electrical recognition of the twenty proteinogenic amino acids using an aerolysin nanopore, Nature Biotechnology. DOI: 10.1038/s41587-019-0345-2
(ID:46293295)






:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d8/94/d8946bebf210c5826a6bfd51d610eedc/0130122950v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ce/d1/ced1a66ddc5248ac5c86aa873b3c8d5a/0131387387v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ba/32/ba322cc757f2f82da2839729e0648ca0/0131377715v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/7a/3e/7a3e9478433a525b34c6b34a0aab133f/0131322665v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/14/59/14590acbf17f99545741a47daa2c66e1/5u3a3997-6720x3778v1.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/27600/27667/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/6400/6447/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/67/49/6749e1ed03ca4/spt-logo-pink-black-01--2-.png)
:quality(80)/p7i.vogel.de/wcms/b7/5b/b75b52a54202a4e6138f3fa06c4255fd/0127814453v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/d5/0d/d50d5dcfe190f840f4e966345755dad6/0124996716v1.jpeg)