Elektronenspinresonanzspektroskopie Aufklärung multivalenter Bindungsmechanismen
Ein neuer Ansatz nutzt Elektronenspin-resonanzspektroskopie, um Bindungsmechanismen zwischen Kohlenhydraten und Proteinen strukturbasiert zu untersuchen. Über Abstandsmessungen können Informationen über das Bindungsverhalten in Lösungen gewonnen werden.
Anbieter zum Thema
Kohlenhydrate sind gemeinhin als Nahrungsmittel oder als Gerüst- und Stützsubstanzen bekannt. Sie besitzen jedoch auch andere Funktionen: So sind sie in Form von Zuckerstrukturen auch auf Zelloberflächen zu finden, wo sie als Erkennungsmuster und damit zur Signalübermittlung dienen. Über diese Zuckerstrukturen können Zellen miteinander kommunizieren. Die Informationsübermittlung findet über die Anbindung dieser Kohlenhydrat-Liganden an Proteine statt. Die Anbindung erfolgt jedoch meist nicht ausschließlich über eine einzelne Bindungsstelle; häufig nutzt der Ligand gleich mehrere Bindungsstellen, um multivalent an das Protein anzudocken. Verglichen mit monovalenten Wechselwirkungen kann solche Multivalenz zu deutlich erhöhter Bindungsaffinität und -spezifität führen. Die zugrunde liegenden molekularen Prozesse sind jedoch noch nicht vollständig verstanden. Verschiedene Mechanismen, insbesondere das überbrückende Binden benachbarter Bindungsstellen, wurden zur Erklärung der erhöhten Bindungsaffinität postuliert.
In vielen biologischen Systemen werden Wechselwirkungen zwischen multivalenten Kohlenhydratderivaten und Lektinen, also Proteinen, die spezifisch Kohlenhydratstrukturen binden, beobachtet. Die Inhibition dieser Wechselwirkungen mittels maßgeschneiderter Liganden ist z.B. von großem Interesse bei der Behandlung vieler Krankheiten.
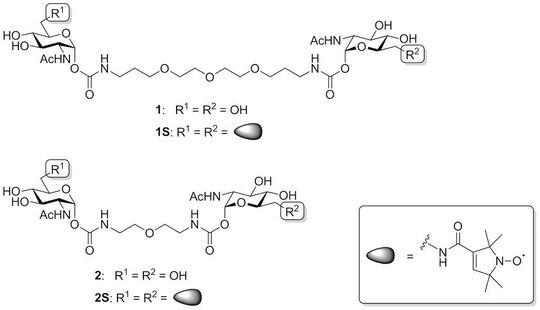
Bisher wurden multivalente Bindungsprozesse meist in kristallinen Proben mithilfe von Röntgenbeugung untersucht, so auch die Bindung von divalenten N-Acetylglucosamin-Derivaten (GlcNAc) an das Pflanzenlektin Weizenkeimagglutinin (WGA). WGA liegt als Dimer vor und besitzt in dieser Form acht Bindungsstellen für GlcNAc. In den untersuchten divalenten Liganden 1 und 2 sind zwei GlcNAc-Reste über einen flexiblen Linker mit variabler Länge miteinander verbunden (s. Abb. 1). Da jedoch die Kristallstruktur von Biomolekülen nicht zwangsläufig deren Struktur in Lösung entspricht und auch der Bindungsmechanismus durch die dichte Packung in einem Kristall beeinflusst werden kann, ist die Untersuchung der multivalenten Wechselwirkungen in Lösung von großer Bedeutung und gleichzeitig eine Herausforderung.
ESR-Spektroskopie und ortsspezifische Spinmarkierung
Eine neue Methode auf Grundlage der Elektronenspinresonanzspektroskopie (ESR-Spektroskopie) ermöglicht, den exakten Bindungsmodus in Lösung zu bestimmen. Dazu werden an den beiden bindungsfähigen Enden der so genannten zweizähnigen Liganden Spinmarker angebracht, die ein ESR-Signal aufweisen (Verbindungen 1S und 2S in Abb. 1). Damit wird die Einschränkung der ESR-Spektroskopie, nur ungepaarte Elektronen detektieren zu können, zum Vorteil für die vorgestellte Methode. Zur Untersuchung der Wechselwirkungen in einem komplexen System aus multivalenten Kohlenhydratderivaten und Lektinen kann das Signal direkt den spinmarkierten Liganden zugeordnet werden.
Mit ESR-Spektroskopie können Abstände zwischen 1 und 10 nm zwischen diesen Spinmarkern gemessen werden. Bei geeigneter Datenanalyse sind auch Abstandsverteilungen zugänglich, sodass auch flexible Strukturen oder parallel vorliegende Konformationen untersucht werden können. Während für die komplementäre Technik FRET (Förster-Resonanzenergietransfer), die zur Abstandsmessung in Proteinen weit verbreitet ist, zwei unterschiedliche, vergleichsweise große Chromophore benötigt werden, die darüber hinaus noch entsprechend dem erwarteten Abstand ausgewählt werden müssen, kommen ESR-Abstandsmessungen mit zwei kleinen, identischen Spinmarkern aus, die über einen großen Abstandsbereich präzise Messungen ermöglichen. Als Spinmarker werden Nitroxide verwendet. Das ungepaarte Elektron, das für die ESR-Spektroskopie benötigt wird, ist dabei über die N-O-Bindung delokalisiert. Die Stabilität der Nitroxide wird vor allem durch die sterische Abschirmung des ungepaarten Elektrons durch Methylgruppen erreicht. Diese kleinen Nitroxidspinmarker üben nur minimalen Einfluss auf die Struktur des Liganden aus. Nichtsdestotrotz sind, wie bei allen Untersuchungen, die mit Labeln arbeiten, Kontrollexperimente unerlässlich.
(ID:30987070)






:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d8/94/d8946bebf210c5826a6bfd51d610eedc/0130122950v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0131240119v5.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/4c/3c4c43bf567ff12c14920f6a8990edcb/0131229738v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3d/c2/3dc269b3435d97799061920f4a281393/0131172010v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fe/3e/fe3e220cf6ac0f453fc75187c04572fd/0130535166v2.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/51400/51447/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/27600/27667/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/67/c9/67c9a358ae891/asecos-box-rot-4c-250x250px.png)
:quality(80)/p7i.vogel.de/wcms/2a/4d/2a4d0da5bc40ca5adc2d99801543eb1a/0128417373v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/f6/c5/f6c5dee27a504a54f331444668311035/0127412932v2.jpeg)