Toxin Aerolysin Bakterien produzieren Biowaffe
Bakterien produzieren einige der giftigsten Substanzen. Molekularbiologen der Universität Bern haben einen Mechanismus entdeckt, der es einem solchen tödlichen Toxin ermöglicht, in menschliche Zellen einzudringen und diese zu zerstören. Ihre Erkenntnisse können dazu beitragen, Gegenmittel zu solchen Giften zu entwickeln.
Anbieter zum Thema
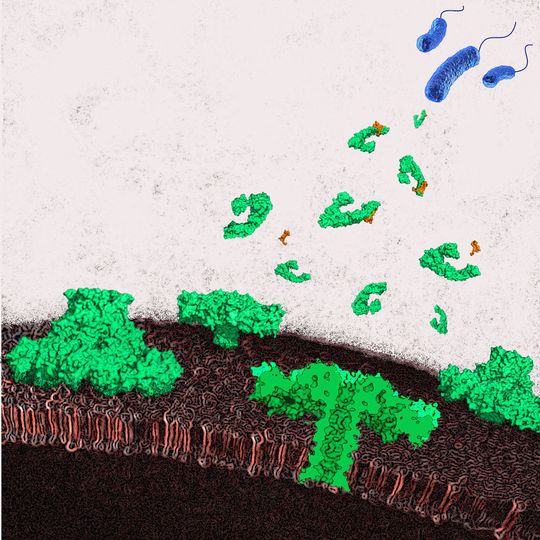
Bern/Schweiz – Pathogene Bakterien produzieren eine Vielzahl von Toxinen, um ihre Wirte anzugreifen. Einige dieser Gifte werden auch als potenzielle Bioterrorismus-Waffen eingestuft. Ein besonders effizientes Toxin kann Löcher in die Membran von Wirtszellen bohren und diese so zerstören. Dieses so genannte porenbildende Toxin findet sich in einer Vielzahl von Bakterien.
Bakterien der Gattung Aeromonas hydrophila produzieren ein porenbildendes Toxin namens Aerolysin. Indem diese Bakterien Zellen in der Darmschleimhaut ihres Wirts angreifen – oder Zellen, die sich an der Oberfläche einer offenen Wunde befinden – können sie sich mittels Aerolysin vom Inhalt der zerstörten Zellen ernähren und noch tiefer in den menschlichen Körper eindringen. Als Folge von zerstörten Darmschleimhaut-Zellen leiden Patienten unter schwerer Diarrhöe. A. hydrophila kann auch schwere Wundinfektionen und Blutvergiftung beim Menschen auslösen.
Neben ihrer pathogenen Funktion sind Aerolysin und andere porenbildende Toxine für die Forschung wegen einer außergewöhnlichen Eigenschaft interessant: Sie werden vom Bakterium als wasserlösliche Proteine abgesondert, die sich dann ineinanderfügen und in die Membran der Wirtszelle eindringen, um sich dort in ein Membranprotein zu verwandeln.
Der Mechanismus, der dem Toxin diese Verwandlung ermöglicht, war bislang unbekannt und wird rege erforscht. Nun ist es einer internationalen Gruppe von Molekuarbiologen unter Führung der Universität Bern und mit Beteiligung der EPFL gelungen, die atomare Struktur von Aerolysin vor, während und nach dem Eindringen in die Zellmembran zu entschlüsseln. Durch die Erkenntnisse lässt sich die Funktion einer großen Kategorie von Toxinen deutlich besser verstehen.
Zerstörung der Zelle in vier Schritten
„Aerolysin ist ein sehr stabiles Toxin“, sagt Prof. Benoît Zuber vom Institut für Anatomie der Universität Bern, der das Projekt zusammen mit Dr. Ioan Iacovache vom selben Institut leitete. „Diese Stabilität des Toxins beruht auf seiner ungewöhnlichen Kernstruktur, welche wir als doppelkonzentrisches Beta-Fass bezeichnen“. Diese macht es der Wirtszelle unmöglich, den Schaden zu reparieren, der aus dem porenbildenden Aerolysin entsteht. „Dies ist auch der Grund, weshalb Aerolysin-ähnliche Toxine zu den wirksamsten porenbildenden Toxinen gehören, die wir kennen“, sagt Zuber.
In einem ersten Schritt dockt das wasserlösliche Toxin mit seiner speziellen Kernstruktur an der Zelloberfläche an. In einem zweiten Schritt wandelt sich ein Teil des Proteins um und bildet einen molekularen Pfeilbogen. Dann kollabiert das Toxin, wodurch der Pfeil in die Zelle geschossen wird – und dabei einen molekularen Tunnel durch die Membran öffnet. Schlussendlich biegt sich die Spitze des Pfeils zu einem Haken und verankert so das Toxin fest in der Membran. „Aerolysin kann sich transformieren wie ein Verwandlungskünstler“, sagt Zuber. „Diese Wandlungen zu verstehen, wird sehr nützlich sein, um neue und wirksamere Therapien gegen Aeromonas-verursachte Krankheiten zu entwickeln“, ergänzt Iacovache.
Wichtig für die DNA-Analyse und die Erforschung von Krankheitsursachen
Wie wegweisende Forschungsergebnisse von anderen Gruppen im Bereich der Nanotechnologie gezeigt haben, kann Aerolysin auch als sehr leistungsfähiges Werkzeug eingesetzt werden, um DNA zu sequenzieren. Zudem wird vermutet, dass bestimmte Proteine unter speziellen Bedingungen eine ähnliche Struktur wie die beschriebene Aerolysin-Struktur bilden. Diese Proteine gehören zu den Auslösern der Alzheimer-Krankheit.
Proteine in atomarer Auflösung sichtbar machen
Mit der Einführung einer neuen Generation von Digitalkameras für Elektronenmikroskope – den so genannten Direktelektronen-Detektoren – können Forschende nun seit vier Jahren die Struktur von Proteinen visualisieren und bestimmen, wie deren Atome angeordnet sind. Solche Details konnten zuvor nur mittels zweier Methoden sichtbar gemacht werden, der Röntgenkristallographie und der Kernspinresonanzspektroskopie (NMR). Die erstere benötigt jedoch Kristalle des zu untersuchenden Proteins, was im Fall von Membranproteinen schwierig ist. Die zweite Methode beschränkt sich auf sehr kleine Proteine.
„Die neue Elektronenmikroskopie-Methode ist ein Durchbruch in der Biomedizin – dank ihr konnte die atomare Struktur einer ganzen Reihe von Proteinen entschlüsselt werden“, sagt Zuber. Die so genannte Kryo-Elektronenmikroskopie, in der Proben schockgefroren werden, um sie besser abbilden zu können, wurde bereits in den 80er Jahren entwickelt und laufend verbessert – so auch in den 90er Jahren an der Universität Bern. Revolutioniert wurde die Methode schließlich mit der Einführung der sehr viel präziseren Digitalkameras.
Originalpublikation: Ioan Iacovache, Sacha De Carlo, Nuria Cirauqui, Matteo Dal Peraro, Gisou van der Goot, Benoît Zuber: Cryo-EM structure of aerolysin variants reveals a novel protein fold and the pore formation process, Nature Communications, 13. Juli 2016, doi: 10.1038/NCOMMS12062
(ID:44167947)







:quality(80)/p7i.vogel.de/wcms/63/2b/632b7c3001c517c32711dac6298f8707/0131501813v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/26/d4/26d4f76786d5636186b53e0460f122ad/0131515490v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/39/fe/39fe2cd50f7947927c078ad83987abf2/microbiome-04-jpg-2cqtransformid-3d15081-2casite-3ddefaultde-pagespeed-ce--ofz-tqfod-750x422v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/cd/e5/cde57faefc6531041e587a2fde0220ef/image1-1322x744v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/13/8f/138f41de403c0c81139657dae230188d/0131503024v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a0/4d/a04d0563072b334bd4cdc0b5ce498763/0131540240v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/d5/d1d5f369ad43bff37d037f8319c35488/img-5661-jpg-2016x1134v1.webp)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/57/11/5711ba14776b6e702c9e775a14837239/0131582930v2.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/6400/6447/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/86900/86921/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/66/38/6638caed1ac07/berner-logo-grey-rgb-v1.png)
:quality(80)/p7i.vogel.de/wcms/71/7a/717aaa3ac94cbe91abd193385f2d72d2/0126196604v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/f8/f9/f8f978c0b112b484f6c1d8f098cf4d9e/0128505849v2.jpeg)