Gentechnik: Schneller und kostengünstiger klonieren Klonierung ohne Screening
Die Klonierung von DNA-Fragmenten ist essentiell für viele Bereiche der Molekularbiologie, Biochemie oder Biotechnologie. Forscher der Universität Bayreuth haben das Verfahren nun beschleunigt und vergünstigt, indem sie das dafür eigentlich notwendige Screening von Bakterienkolonien überflüssig machen. Wie ihnen das gelungen ist, zeigt der folgende Beitrag.
Anbieter zum Thema
Bayreuth – Die DNA ist wohl das fundamentalste aller Makromoleküle, trägt sie doch die Erbinformation aller Lebewesen. Zu Recht wird sie daher häufig als „Bauplan des Lebens“ bezeichnet. Um zu erforschen, welche DNA-Abschnitte welche Funktion haben, müssen die entsprechenden DNA-Fragmente vervielfältigt werden. Allen Verfahren, die derzeit zu einer solchen Klonierung eingesetzt werden, ist gemeinsam, dass diese Fragmente zunächst in größere Trägermoleküle, Vektoren genannt, eingebaut werden. Die mit DNA-Fragmenten beladenen Vektoren werden anschließend in Bakterien eingeschleust. Diese erledigen dann die entscheidende Arbeit. Denn indem sie sich vermehren und so eine Bakterienkolonie bilden, vervielfältigen sie auch die DNA-Fragmente tausendfach.
Bisher haben diese Verfahren einen wesentlichen Nachteil: Trotz moderner Präparationsmethoden gelingt der Einbau von DNA-Fragmenten in das Trägermolekül nicht immer störungsfrei und mit der nötigen Perfektion. Daher besitzen keineswegs alle, sondern nur einige Kolonien die Vektoren mit den zu vervielfältigenden DNA-Fragmenten. Um diese „Erfolgsfälle“ zu identifizieren, war bisher ein zeitaufwändiges und teures Screening unvermeidlich.
Gift-Gen als Erfolgsgarant
Forschern der Universität Bayreuth unter der Leitung von Prof. Dr. Stefan Schuster ist es jetzt gelungen, dieses Screening überflüssig zu machen, indem sie Fehler beim DNA-Transfer direkt eliminieren. Das gelingt ihnen, weil sie ein Plasmid als Vektor verwenden, das in seiner Ringstruktur ein toxisches Gen enthält.
Beim Einbau der DNA-Fragmente visieren die Forscher dieses toxische Gen an, um es mit dem Fragment zu ersetzen. Nach erfolgreichem Transfer ist das Vektor-Plasmid also sozusagen entgiftet. Gelingt das nicht, bleibt das toxische Potenzial im Plasmid erhalten. Wird solch ein Plasmid in ein E. coli-Bakterium eingeschleust, setzt die toxische Wirkung ein: Sie macht das Bakterium vermehrungsunfähig sorgt dafür, dass es nicht lange überlebt.
Durch diesen Kontrollmechanismus ist von vornherein gewährleistet, dass nur solche E.-coli-Bakterien Kolonien bilden, in denen die DNA-Fragmente tatsächlich enthalten sind. Sie müssen nicht nachträglich ausgelesen werden. „Unser neues Klonierungssystem ist vor allem deshalb so effizient, weil die Auslese der mit klonierten DNA-Fragmenten ausgestatteten Bakterien zuverlässig von selbst erfolgt. Die vervielfältigten Plasmide können aus diesen Bakterien isoliert und weiterverwendet werden – sei es, um die klonierte DNA zu analysieren oder um sie für die biotechnologische Herstellung von Proteinen einzusetzen“, sagt der Bayreuther Biologe Dr. David Richter, Erstautor der Studie.
Weiterer Fortschritt: DNA-Kleber
Das neue Verfahren des Bayreuther Forscherteams vereinfacht die Klonierung noch in einer weiteren Hinsicht: Die Wissenschaftler haben einen aus den Zellen von E.-coli-Bakterien gewonnenen Extrakt (SLiCE) so optimiert, dass er sich hervorragend als „Klebstoff“ eignet, um mehrere DNA-Fragmente wie die Glieder einer Kette aneinanderzureihen und zu verbinden. So können jetzt die verschiedensten Kombinationen von DNA-Fragmenten in das Plasmid eingefügt werden – und zwar deutlich schneller als mit bisherigen Methoden, wie die Forscher berichten.
Das Team um Schuster hat das neue Klonierungssystem auf den Namen ZeBRα getauft. Das Akronym leitet sich von den wissenschaftlichen Bezeichnungen der beiden entscheidenden Faktoren ab: Zum einen von dem verwendeten Plasmid, einem Zero Background Vektor, der keine störenden Bakterienkolonien ohne erfolgreich eingebautes DNA-Fragment zulässt. Zum anderen von der Redα-Exonuclease, einem Bestandteil des DNA-Klebers aus dem E.-coli-Extrakt.
Fluoreszenz als Erfolgskontrolle
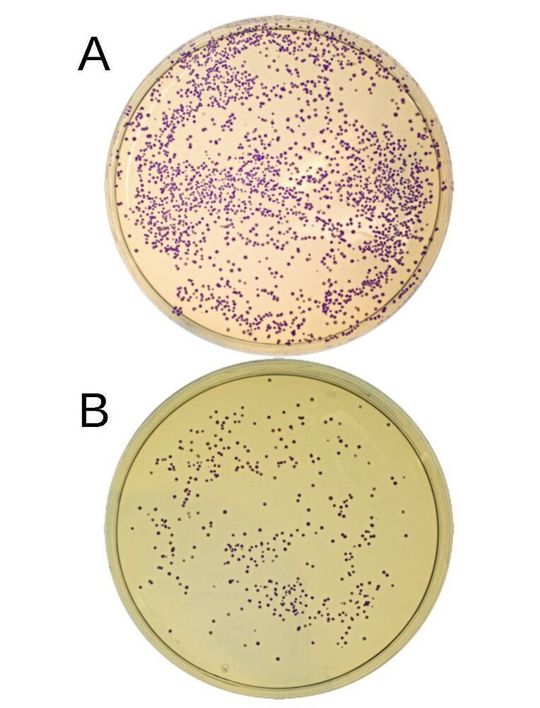
Anknüpfend an die jetzt veröffentlichten Forschungsergebnisse wollen die Wissenschaftler ihr Klonierungsverfahren künftig um weitere Funktionen bereichern und dadurch vielseitiger einsetzbar machen. Insbesondere soll der Vektor so optimiert werden, dass er die Transformation bestimmter Organismen oder Zelllinien erleichtert. Dabei werden DNA-Fragmente direkt in Organismen oder Zellen übertragen. Weil auch diese Übertragung relativ selten zustande kommt, ist es vorteilhaft, wenn der Vektor DNA-Sequenzen mitbringt, die zur Bildung fluoreszierender Proteine führen. Diese Proteine machen dann den erfolgreichen Einbau der DNA-Fragmente sichtbar (vgl. Abb. links).
Originalpublikation: David Richter, Katharina Bayer, Thomas Toesko, Stefan Schuster: ZeBRα a universal, multi-fragment DNA-assembly-system with minimal hands-on time requirement. Scientific Reports 9 (2019); DOI: 10.1038/s41598-019-39768-0
* C. Wißler, Universität Bayreuth, 95447 Bayreuth
(ID:45803292)






:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d8/94/d8946bebf210c5826a6bfd51d610eedc/0130122950v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ce/d1/ced1a66ddc5248ac5c86aa873b3c8d5a/0131387387v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ba/32/ba322cc757f2f82da2839729e0648ca0/0131377715v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/7a/3e/7a3e9478433a525b34c6b34a0aab133f/0131322665v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/2f/38/2f3820f7397d7727ab6e3bdf80d4f775/0131487405v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/2e/17/2e1795b6750cc3eaad6ba81c0bc79d16/0100811496v7.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/27600/27667/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/69/2e/692ed0d59df43/a1sciences-4c-transparenter-hintergrund.png)
:fill(fff,0)/p7i.vogel.de/companies/67/49/6749e1ed03ca4/spt-logo-pink-black-01--2-.png)
:quality(80)/p7i.vogel.de/wcms/f6/c5/f6c5dee27a504a54f331444668311035/0127412932v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/68/02/680272d28efb89d85e65d8bb07de7e93/0130542168v2.jpeg)