Güte einer UHPLC-Trennung Strategie zum Screenen von UHPLC-Säulen
Wovon hängt die Güte einer UHPLC-Trennung ab? Lesen Sie, wie eine auf QbD-Prinzipien basierende Methode zur Beurteilung der Güte herangezogen werden kann, die neben der Auflösung des kritischen Peakpaares auch die Robustheit der Trennung betrachtet.
Anbieter zum Thema
[Am Ende des Artikels können Sie sich eine ausführliche Ausarbeitung zu diesem Thema herunterladen.]
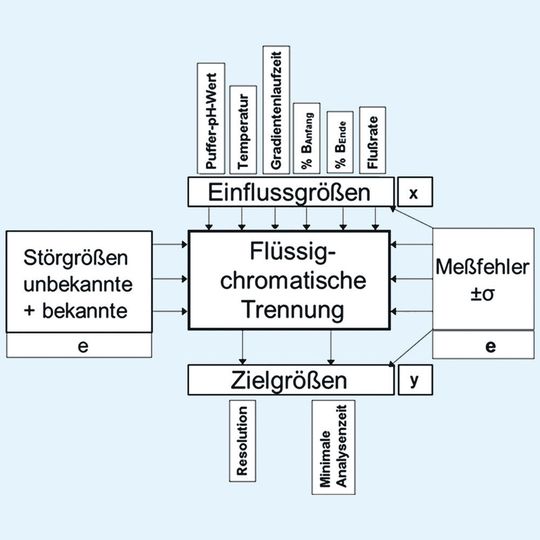
Die Qualität eines flüssigchromatographischen Trennprozesses hängt von einer Vielzahl von Faktoren und Zielgrößen ab. In der pharmazeutischen Analytik von kleinen Molekülen können je nach Molekül für die UHPLC-Trennungsoptimierung bis zu zehn Faktoren sowie deren Wechselwirkungen signifikant sein. Solche Faktoren sind zu suchen in der Gradientenzeit (tG), der Temperatur (T), der ternären Eluentzusammensetzung (tC) des organischen Eluenten B, der Startkonzentration (%Bs) und Endkonzentration (%Be) des organischen Eluenten B, dem pH des wässrigen Eluenten A (pH) sowie der Flussrate (F). Nicht zu vergessen ist natürlich die stationäre Phase der Trennsäule selbst als wichtige Einflussgröße. Zielgrößen sind zu sehen in der kritischen Auflösung Rs,krit. (Auflösung für das am schlechtesten getrennte Peakpaar im Chromatogramm) für die optimale UHPL-Trennung sowie in der Retentionszeit des letzten Peaks im Chromatogramm tRmax. zur Minimierung der Analysenzeit. Die Minimierung der Analysenzeit von Routinemethoden bietet ein erhebliches Potenzial zur Steigerung des Durchsatzes und der Produktivität im UHPLC-Analysenlabor.
Kommerziell erhältliche Software zur Computer-unterstützten UHPLC-Methodenentwicklung (CMD) wie etwa Drylab (Molnar-Institut für angewandte Chromatographie) oder Chromsword (VWR International) unterliegen den Einschränkungen einer maximal 3-Faktor-Optimierung sowie der Modellierung mit nur einer Zielgröße (Auflösung des kritischen Peakpaares). Es wird am „globalen Optimum“ vorbei optimiert [1], ohne dass eine Diagnostik oder auch nur eine Strategie existiert, um dies zu erkennen und zu verbessern.
Ein mehr als drei Methodenparameter sowie mehr als eine Zielgröße umfassendes Screenen einer UHPLC-Trennung ist durch Verknüpfung der sehr effektiven Arbeitsweisen von Computer-unterstützter UHPLC-Trennoptimierung (chromatographische Modellierungssoftware z.B. Drylab 4) und statistischer Versuchsplanung (statistische DoE-Software z.B. Modde 11 Pro) realisierbar [2].
Experimentelles
Die Versuche wurden von Robert Kormany (Egis Pharmaceuticals) und Imre Molnar und H.-J. Rieger (Molnar Institut) durchgeführt. Die Versuchsparameter waren:
- Säule: UHPLC-Säulen der Dimension 50 x 2,1 mm mit 2-µm-Partikel.
- Eluent: Die mobile Phase war eine Mischung von Acetonitril und 5 mM Ammoniumdihydrogenphospat-Puffer. Der Analyt enthält 10 µg/ml Amlodipin und seine Ph.Eur.-Verunreinigungen (A, B, D, E, F, G und H), gelöst in Acetonitril:Wasser (30:70)(V/V)).
Für neun unterschiedliche UHPLC-Säulen wurden jeweils vier chromatographische Trennungen (linearer Gradient 30 - 90%B, Gradientenzeit 3 min und 9 min, Temperatur 15 °C und 45 °C) bei drei verschiedenen pH-Werten (2,0, 2,5, 3,0) des phosphatpufferhaltigen Eluenten A auf einem Shimadzu LC-2010C (Verweilvolumen 1,06 ml) ausgeführt. Detektiert wurde bei 254 nm. Das Injektions-Volumen betrug 1 µl [3].
Empirisches Prozessmodell
Ableitend aus den Rohdaten dieser 3-Faktor-Optimierung (zur Verfügung gestellt vom Molnar-Institut für Chromatographie), wurde für die simultane Optimierung aller signifikanten UHPLC-Methodenparameter jeweils ein empirisches Prozessmodell (s. Abb. 1) [4, 5] mit sechs Faktoren und mehreren Zielgrößen für drei UHPLC-Säulen aufgestellt, abgearbeitet und visualisiert. Zum robusten Screenen wurde die sehr effiziente Arbeitsweise der statistischen Versuchsplanung (DoE) benutzt. Basierend auf den Ergebnissen der statistischen Versuchsplanung wird ein empirisches, statistisch abgesichertes Prozessmodell erstellt und nach Modell-Überprüfung mit einfachen statistischen Diagnosen (Residuenanalysen) ein Screening durchgeführt. Dabei treten häufig Zielkonflikte auf. Einstellungen der Faktoren, die für eine Zielgröße günstig sind, können für andere Zielgrößen ungünstig sein. Um robust zu screenen, ist also ein Multi-Zielgrößen-Modell notwendig [6]. Den Bereich, den alle Faktoren von ihrer minimalen bis zu maximalen Einstellung abdecken, nennt man Versuchsraum, im Kontext von QbD auch Knowledge Space. Er ist i.d.R. wesentlich größer als der anschließend zu bestimmende Design Space [7]. Meist benötigt man mehrere Zielgrößen, um alle Ziele einer Versuchsreihe abzubilden. Die Auflösung des kritischen Peakpaares wird auch heute noch als alleinige Zielgröße einer UHPLC-Trennung angesehen [8].
Artikelfiles und Artikellinks
(ID:44261245)






:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d8/94/d8946bebf210c5826a6bfd51d610eedc/0130122950v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ce/d1/ced1a66ddc5248ac5c86aa873b3c8d5a/0131387387v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ba/32/ba322cc757f2f82da2839729e0648ca0/0131377715v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/7a/3e/7a3e9478433a525b34c6b34a0aab133f/0131322665v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/2e/17/2e1795b6750cc3eaad6ba81c0bc79d16/0100811496v7.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/69/67/696769fab6999/kern-logo2023-blau-4c-or.png)
:fill(fff,0)/p7i.vogel.de/companies/67/c9/67c9a358ae891/asecos-box-rot-4c-250x250px.png)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/69800/69835/65.jpg)
:quality(80)/p7i.vogel.de/wcms/68/04/68042597b0987dc4d57c3b541f8e3b16/0128181173v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/f5/ea/f5ea9b22a7e3774b8ca8a19e9db95915/0131239927v10.jpeg)