Killerzellen zur Behandlung von Hautverletzungen Balance zwischen Wundheilung und Bakterienabwehr
Natürliche Killerzellen sind im Körper nicht nur für zerstörerische Aufgaben zuständig. So zeigt eine neue Studie von Forschern der Universität Zürich, dass sie auch eine wichtige Rolle bei der Wundheilung spielen. Wenn die Killerzellen allerdings zu stark zur Wundheilung angetrieben werden, geht dies auf Kosten ihrer Funktion in der Bakterienabwehr.
Anbieter zum Thema
Zürich/Schweiz – Natürliche Killerzellen sind ein bestimmter Typ von Immunzellen. Sie erkennen abnormale Körperzellen wie Tumor- und virusinfizierte Zellen und töten diese ab. Ein internationales Forschungsteam unter der Leitung von Christian Stockmann, Professor am Institut für Anatomie der Universität Zürich (UZH), hat nun herausgefunden, dass Killerzellen eine weitere, überraschende Funktion haben: Sie kontrollieren die Wundheilung in der Haut. „Wir konnten diese Zellen in Mäusen genetisch so verändern, dass das Wachstum von Blutgefäßen beschleunigt wird und sich Hautwunden schneller schließen. Allerdings wird dadurch die Immunabwehr abgeschwächt, was die Anfälligkeit für bakterielle Infektionen erhöht“, sagt Stockmann.
Schneller heile, schneller infektiös?
In der Biomedizin wird intensiv nach Möglichkeiten gesucht, um Wundheilungsprozesse zu beeinflussen. Wissenschaftler versuchen v. a., die Gefäßneubildung anzuregen und zu beschleunigen – entweder direkt oder indirekt über die Beeinflussung der Immunantwort. „Unsere Ergebnisse zeigen, dass man bei solchen Ansätzen möglicherweise ein erhöhtes Infektionsrisiko in Kauf nimmt. Daher ist hier Vorsicht geboten“, erklärt Stockmann.
Eine weitere offene Frage ist, inwiefern natürliche Killerzellen nicht nur das Tempo, sondern auch die Qualität der Wundheilung beeinflussen – etwa die Zusammensetzung des Bindegewebes oder die Regeneration von Haarfollikel, Drüsen und anderen Hautkomponenten. „Die spannendste Frage ist, wie wir es schaffen können, die Wundheilung zu beschleunigen und gleichzeitig die Immunabwehr gegen Wundinfektionen zu stärken“, sagt der Anatom und Immunologe Stockmann.
Killerzellen als Abwehr gegen antibiotikaresistente Bakterien
Der Wissenschaftler sieht aber noch weiteres Potenzial: Bei Krebstherapien werden heute auch Therapeutika eingesetzt, die Killerzellen aktivieren und stimulieren, sodass diese vermehrt die Krebszellen abtöten. „Unsere Daten weisen darauf hin, dass diese Medikamente auch bei bakteriellen Infektionen nützlich sein könnten – was angesichts der zunehmend antibiotikaresistenten Keime unbedingt weiter erforscht werden sollte.“
:quality(80)/images.vogel.de/vogelonline/bdb/1868800/1868876/original.jpg)
3D-gedrucktes, smartes Pflaster
Grünes Licht für schnelle Wundheilung
Natürliche Killerzellen kommunizieren laufend mit anderen Abwehrzellen und beeinflussen deren Aktivität. Dazu sondern sie Botenstoffe ab, so genannte Zytokine. In ihrer Studie stellten die Forscher fest, dass Killerzellen auch Hautverletzungen infiltrieren, in denen sehr niedrige Sauerstoffkonzentrationen herrschen. In solchen Geweben stellen Killerzellen ihre Genaktivität um und passen sich so dem Sauerstoffmangel an.
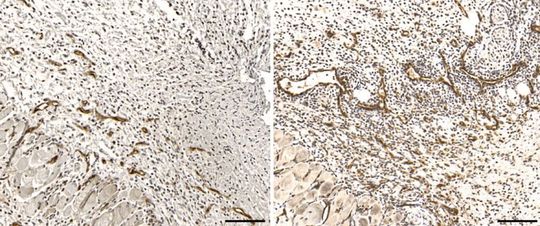
Verantwortlich für diese Umstellung sind so genannte HIF-Signalfaktoren. Fehlt in Mäusen einer dieser Signalfaktoren, ist die Ausschüttung bestimmter Zytokine beeinträchtigt. Als Reaktion darauf wird das Wachstum von Blutgefäßen in der Haut und damit die Wundheilung beschleunigt, während die Bekämpfung bakterieller Infektionen gedrosselt wird. Die Balance verschiebt sich so in Richtung Wundheilung – auf Kosten der Immunabwehr.
Originalpublikation: Michal Sobecki, Ewelina Krzywinska, Shunmugam Nagarajan, et. al.: NK cells in hypoxic skin mediate a trade-off between wound healing and antibacterial defence. Nature Communications volume 12, Article number: 4700 (2021); DOI: 10.1038/s41467-021-25065-w
(ID:47641231)







:quality(80)/p7i.vogel.de/wcms/a4/48/a448e4608d93394784d7b364306bc361/0130506959v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/07/29/072962cf54ce048cab6f90214fc58418/image1v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/4a/b6/4ab66927b81ebf966a41081699111fdc/0131598871v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/6c/93/6c93b004f1e78deb7e24da3318766f84/0131138303v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/9a/7e/9a7e5bdb654d5b666a01cf46483c8fc7/adobestock-1995567901-editorial-use-only--c2-a9-20stephen-20-e2-80-93-20stock-adobe-com-4000x2251v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/26/d4/26d4f76786d5636186b53e0460f122ad/0131515490v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/81/08/8108a3770d79143e5eb43b42fd28766d/0131718320v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/7b/c9/7bc945fec5ec26d7c154890235f42e31/0131662861v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/1b/a2/1ba2d027a8c41332bd5ac2f897250113/0131662713v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/c7/92/c792a20f82cca86e2414ee97590b3b29/0131648572v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/b9/c7/b9c7ab7ddb6e2b3a4f9a2b40541de5f0/0131675956v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/31/9f/319fb620749d359ee20c28483338dc0e/0131664573v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/a0/4d/a04d0563072b334bd4cdc0b5ce498763/0131540240v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/d5/d1d5f369ad43bff37d037f8319c35488/img-5661-jpg-2016x1134v1.webp)
:quality(80)/p7i.vogel.de/wcms/2e/17/2e1795b6750cc3eaad6ba81c0bc79d16/0100811496v7.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/115900/115965/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/90100/90188/65.png)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/40400/40477/65.jpg)
:quality(80)/p7i.vogel.de/wcms/0d/e2/0de2ad009e7d7da55cddbe296a647495/0129265791v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/1b/15/1b15246ce31f5c6dfbb577a51033ef30/0126692823v1.jpeg)