Flüssigchromatographie Bessere Effizienz in der HPLC durch Temperaturerhöhung?
Anbieter zum Thema
Der Druck ist in der HPLC sicherlich der physikalische Parameter, den die Anwender immer im Blick haben, wenn es um die Effizienz einer Trennung geht. Lesen Sie, welche Auswirkungen Temperaturänderungen bei der Flüssigchromatographie haben.
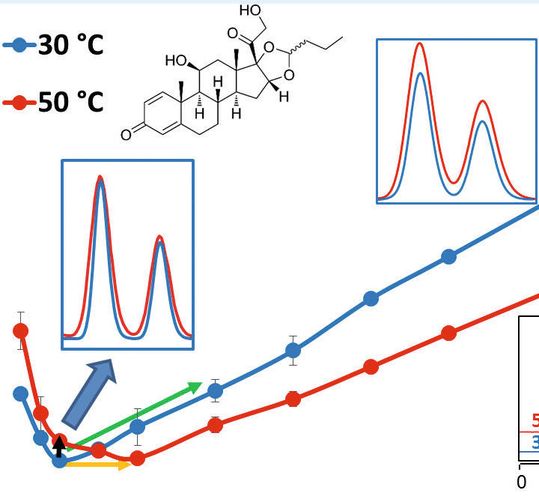
In der Chromatographie wie der HPLC wirkt sich die Temperatur einerseits auf Retention und Selektivität aus, andererseits auf die für die Geschwindigkeit und Effizienz von Trennungen wichtigen Massentransportprozesse. Diese kinetischen Aspekte von Temperaturänderungen werden hier praxisnah beleuchtet.
Die van-Deemter-Gleichung (1) beschreibt den Zusammenhang zwischen Bandenverbreiterung oder Dispersion in der Trennsäule (gemessen als Bodenhöhe H) und Lineargeschwindigkeit u der mobilen Phase, also Geschwindigkeit der Trennung. Sowohl bei der axialen Verbreiterung des Peaks durch Diffusion (Longitudinaldiffusion, B-Term) als auch beim Massentransport des Analyten zwischen mobiler und stationärer Phase (C-Term) spielt der Diffusionskoeffizient Dm eine entscheidende Rolle und er steigt mit zunehmender Temperatur. Interessant ist dabei, dass sich die Longitudinaldiffusion zwar verstärkt (negativer, Peak-verbreiternder Effekt), der beschleunigte Massentransport die Trennung bei hohen Geschwindigkeiten aber günstig beeinflusst (positiver Effekt).
Melden Sie sich an oder registrieren Sie sich und lesen Sie weiter
Um diesen Artikel vollständig lesen zu können, müssen Sie registriert sein. Die kostenlose Registrierung bietet Ihnen Zugang zu exklusiven Fachinformationen.
Sie haben bereits ein Konto? Hier einloggen







:quality(80)/p7i.vogel.de/wcms/63/2b/632b7c3001c517c32711dac6298f8707/0131501813v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/48/0e/480e6d0c7a7a9afe60023e5560c00b30/0131243004v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/f4/96f41136c248248817210b7df8296c6e/0131243044v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/26/d4/26d4f76786d5636186b53e0460f122ad/0131515490v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/b5/43b5b01a01e23c21009d2ca43e73bc5e/0131461156v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/39/fe/39fe2cd50f7947927c078ad83987abf2/microbiome-04-jpg-2cqtransformid-3d15081-2casite-3ddefaultde-pagespeed-ce--ofz-tqfod-750x422v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/cd/e5/cde57faefc6531041e587a2fde0220ef/image1-1322x744v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/13/8f/138f41de403c0c81139657dae230188d/0131503024v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/1f/251fac2058dce921eba03b6e830876ec/0131426881v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a0/4d/a04d0563072b334bd4cdc0b5ce498763/0131540240v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/d5/d1d5f369ad43bff37d037f8319c35488/img-5661-jpg-2016x1134v1.webp)
:quality(80)/p7i.vogel.de/wcms/04/49/044958b43723ceca42410feb766079ae/0131240585v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/57/11/5711ba14776b6e702c9e775a14837239/0131582930v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fb/49/fb49fffcc5b2584659c1a81932ab3c55/0131215424v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/68/04/68042597b0987dc4d57c3b541f8e3b16/0128181173v2.jpeg)