Struktur von Vitamin B12 kristallisiert Ein „Kobold“ in der Vitamin-Spirale
Das für Menschen essentielle Vitamin B12 besitzt eine spiralförmige Struktur mit einem Cobalt-Ion in der Mitte. Nun haben Forscher erstmals die Struktur des metallfreien Grundkörpers des Vitamins bestimmt und abgeleitet, welche Bedeutung die Helix-Struktur für die Katalysewirkung des Vitamins hat.
Anbieter zum Thema
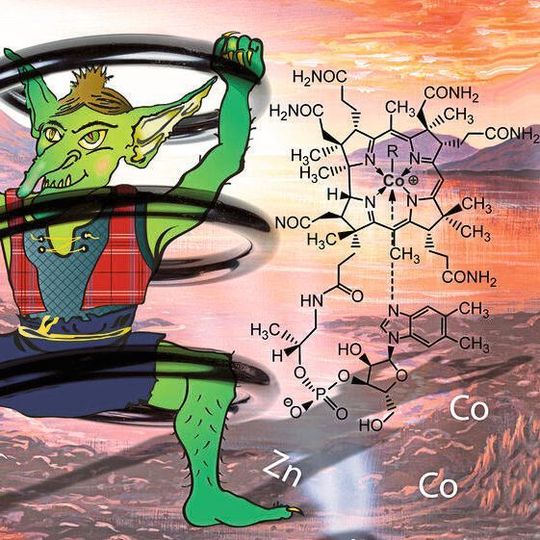
Leipzig – Vitamin B12 ist unter anderem an der Blutbildung und bestimmten Stoffwechselwegen beteiligt und für viele Lebewesen essentiell. Interessanterweise sind nur Mikroorganismen in der Lage, diese biologisch wichtige Verbindung herzustellen. Zwar haben auch Menschen entsprechende Bakterien im Darm, doch für eine ausreichende Versorgung muss der Mensch das Vitamin über die Nahrung aufnehmen, genauer gesagt über tierische Produkte wie Fleisch, Fisch und Eier.
Um die Wirkung des Vitamins näher zu erforschen, ist das Wissen um die Molekülstruktur entscheidend. So haben Forscher bereits herausgefunden, dass im Zentrum der Verbindung ein einzelnes Cobalt-Ion sitzt, weshalb Wissenschaftler manchmal auch vom „Kobold-Vitamin“ sprechen.
Antivitamine durch Metallaustausch
Basierend auf Arbeiten der Forschungsgruppe von Martin Warren an der britischen University of Kent mit genetisch modifizierten Mikroorganismen ist es den Chemikern um Bernhard Kräutler vor einigen Jahren bereits gelungen, das Cobalt-Ion durch ein Rhodium-Ion zu ersetzen. Mit ihren Kooperationspartnern konnten sie nun das intakte metallfreie Kernelement der Vitaminstruktur biotechnologisch erzeugen. „Damit wurde ein Traum vieler B12-Forscher war, da diese Verbindung eine ideale Basis für die nun vergleichsweise direkte Synthese von analogen Verbindungen bietet, in welchen andere Metalle anstelle des aktivierten Cobalt-Ions von Vitamin B12 sitzen“, sagt Kräutler. Solche inaktive ‚Antivitamine B12‘ werden nach Meinung der Forscher interessante Erkenntnisse über die biologischen Funktionsweisen von Vitamin B12 ergeben.
Spirale unter Spannung
Den Innsbrucker Wissenschaftlern ist es erstmals gelungen, die Cobaltfreie Grundeinheit von Vitamin B12 zu kristallisieren. Sie konnten damit genau zeigen, wie die Vitamin-Grundstruktur um das Cobalt-Ion herum spiralförmig angeordnet ist. „Die besondere Reaktivität des Vitamins rührt offenbar daher, dass sowohl das Cobalt-Ion wie auch der es bindende helikale Corrin-Ring strukturbedingt unter Spannung stehen. Für seine Stabilisierung und Entspannung im Komplex spaltet das Cobalt-Ion einen oder seine beiden weiteren Liganden leicht ab, was die Katalyse schon entscheidend auf den Weg bringt“, erklärt Christoph Kieninger, Postdoktorand in Kräutlers Gruppe.
Bisher wusste man, dass der Corrin-Ring speziell auf die Größe der Cobalt-Ionen angepasst ist. Die genau analysierte, spiralförmige Struktur erwies sich nun als ein wichtiger zweiter Strukturfaktor, der aber speziell der Steigerung der Reaktivität des Cobalt-Zentrums des Vitamins für seine Katalysefunktion zu dienen scheint.
:quality(80)/images.vogel.de/vogelonline/bdb/1329500/1329570/original.jpg)
Vitamin-Mangel im Alter
Vitamin D und B12: Studie bestätigt kritische Unterversorgung im Alter
Cobalt in Vitamin B12
Die Grundstruktur von Vitamin B12 als Cobalt-Corrin dürfte erdgeschichtlich schon sehr früh entstanden und dann von ersten lebenden Organismen genutzt worden sein. Im Laufe der Evolution wurde diese Struktur nur durch einfache Modifikationen in den lebenden Zellen weiter verbessert, wobei sich aber Cobalt als das ideale Katalysezentrum für verschiedene wichtige Lebensprozesse erwiesen hat. Deshalb wurde der resultierende Cobaltkomplex, Vitamin B12, für viele Lebewesen unentbehrlich, so auch für den Menschen. Ob und wie andere Metalle als Cobalt die Aktivität so entscheidend verändern, dass sogar inaktive ‚Antivitamine B12‘ entstehen, will Kräutler mit seinem Team als nächstes herausfinden.
Originalpublikation: Christoph Kieninger, Evelyne Deery, Andrew Lawrence, Maren Podewitz, Klaus Wurst, Emi Nemoto-Smith, Florian J Widner, Joseph A Baker, Steffen Jockusch, Christoph R Kreutz, Klaus R Liedl, Karl Gruber, Martin J Warren Bernhard Kräutler: The Hydrogenobyric Acid Structure Reveals the Corrin Ligand as an Entatic State Module Empowering B12‐Cofactors for Catalysis, Angewandte Chemie (2019). DOI: 10.1002/anie.201904713
(ID:45993903)






:quality(80)/p7i.vogel.de/wcms/46/10/46104916e8a69933218fded0d5925feb/0130443323v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c9/16/c9162be8c6014187286dda23e57f8793/0130654555v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/9f/9d/9f9d6fc46606d654deca536f05102f7a/0130752952v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/58/bb58da17d7bb11b44fcae8d06c35df76/0130791510v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0130924147v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a6/e0/a6e0ab14cf7f6b22d536f6ca6e5fb777/0130793394v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/63/85/638523e67603079a004bbd3a99b6ad92/0130856502v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/df/3d/df3d3f7d7b425eabae87bab4ef68bd6c/0130259765v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/b9/32/b9326aa0b6f26d5e5eeee82c86aab8b6/0130976290v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/2d/5f/2d5f14d92ec22f38682c6d240600579f/0131000090v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/19/40/194054b15f3c0e161583d7ea8917ec3f/0130974372v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/e2/5e/e25e2c9f40617e17d32524787c6ece1d/0130248690v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/09/88/09883aaf7db3151a2e894d56c2a515d4/0130982666v2.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/40400/40477/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/68/cc/68cc2bec527f5/hls-logo-2023.png)
:fill(fff,0)/p7i.vogel.de/companies/67/c9/67c9a358ae891/asecos-box-rot-4c-250x250px.png)
:quality(80)/p7i.vogel.de/wcms/e3/30/e330ee3a0e4087ba64dbe78459f6c4b8/0130676797v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/76/fd/76fdd392032917cda2bc39d3cdb7eacb/0124659708v1.jpeg)