Software für Labore im GxP-Umfeld Qualifizierung analytischer Instrumente mit höchster Datenintegrität
Um zuverlässig nach den ALCOA-Richtlinien der amerikanischen Food and Drug Administration (FDA) zu arbeiten, hat das Unternehmen Anatox eine neue Software veröffentlicht. Damit soll die Qualifizierung für Labore im (c)GxP-Umfeld ohne großen Aufwand gewährleistet werden.
Anbieter zum Thema
Für die Qualifizierung von GC/HPLC/MSD Instrumenten hat die Firma Anatox eine neue Software veröffentlicht: AIQ-Tool soll das erste herstellerunabhängige Werkzeug im regulierten Umfeld sein, welches die ALCOA-Richtlinien der amerikanischen Food and Drug Administration (FDA) erfüllt, heißt es in einer Pressemeldung.
- Attributable (zuordenbar):
Das Benutzermanagement definiert klar alle Rollen und Rechte für jeden Anwender. AIQ-Tool kann direkt beim Nutzer installiert werden, weil es keinen „Kontakt“ mit dem qualifizierten CDS (chromatography data system) gibt. Die Benutzung ist limitiert und reguliert durch digital signierte Zertifikate. Nur geschulten und zertifizierten Mitarbeitern ist es erlaubt, die Qualifikation eines Instruments durchzuführen.
- Legible (lesbar):
Die implementierte Datenbank speichert alle Rohdaten, Metadaten und die kompletten Reports. Jeder Report erhält eine Printing-ID, um jede Ausgabe eines Reports zu verfolgen.
- Contemporaneous (zeitnah):
Ein spezieller Reviewer Account erlaubt den vollen Zugriff auf alle Daten, Reports und das komplette Audit-Trail der gesamten Qualifikationshistorie. Die Speicherung der Daten und die Generierung von Reports ist in Übereinstimmung mit den Regularien entsprechend 21 CFR Part 11.
- Original (original):
Eines der Schlüsselfeatures ist der „Level 4“ Hardwaresupport der Instrumente. Mit dieser Hardwaresteuerung wird eine aktive Bestätigung des korrekten Empfangs aller Befehle sichergestellt, um u.a. Fehler zu vermeiden oder zu detektieren. Sie ist verantwortlich für eine garantierte und reproduzierbare Steuerung und Datenaufnahme. Es soll kein Import kritischer Daten notwendig sein: Jede Eingabe von Parametern und das Senden von Befehlen an das entsprechende Modul wird mit dessen Seriennummer im Audit Trail Protokoll registriert.
- Accurate (korrekt):
Typisches Reprozessieren von Daten ist verboten, um jede Manipulation von Daten auszuschließen. Die Parameter-Setups der ausgeführten Prozeduren sind fest; es sind während der Prozedur keine Veränderung möglich, allerdings ist die Anpassung der Limits erlaubt.
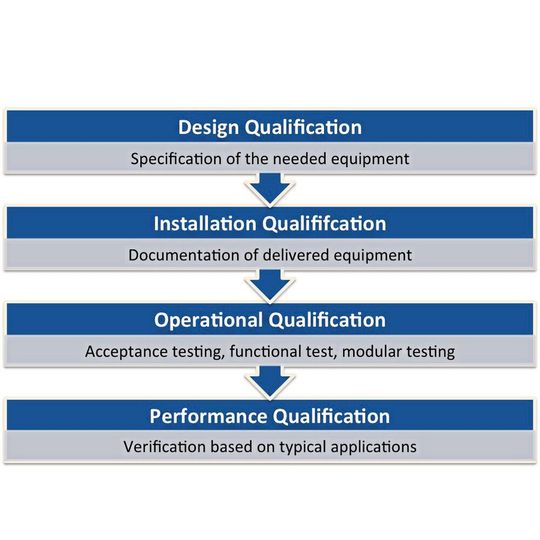
Für Labore im (c)GxP Umfeld werden die Anforderungen entsprechend des USP Kapitels <1058> zur Gerätequalifizierung seit 2008 empfohlen. Die Software hilft, die Geräte zu charakterisieren, indem sie Systemchecks oder vollständige Qualifikationsprozeduren ausführt. Sie bietet alle Optionen der Installations- und Leistungsqualifikation sowie der Qualifikation nach Reparatur.
(ID:46106353)






:quality(80)/p7i.vogel.de/wcms/46/10/46104916e8a69933218fded0d5925feb/0130443323v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c9/16/c9162be8c6014187286dda23e57f8793/0130654555v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/9f/9d/9f9d6fc46606d654deca536f05102f7a/0130752952v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/58/bb58da17d7bb11b44fcae8d06c35df76/0130791510v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0130924147v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a6/e0/a6e0ab14cf7f6b22d536f6ca6e5fb777/0130793394v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/63/85/638523e67603079a004bbd3a99b6ad92/0130856502v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/df/3d/df3d3f7d7b425eabae87bab4ef68bd6c/0130259765v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/b9/32/b9326aa0b6f26d5e5eeee82c86aab8b6/0130976290v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/2d/5f/2d5f14d92ec22f38682c6d240600579f/0131000090v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/19/40/194054b15f3c0e161583d7ea8917ec3f/0130974372v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/e2/5e/e25e2c9f40617e17d32524787c6ece1d/0130248690v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/09/88/09883aaf7db3151a2e894d56c2a515d4/0130982666v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ea/fc/eafc19c5d59b25706790fe14f814eb88/0131009351v3.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/27600/27667/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/69/95/6995807285729/leco-logo-color.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/63/9c/639c7cce17c0a/pce-instruments-logo-300dpi.png)
:quality(80)/p7i.vogel.de/wcms/df/2e/df2e74a397344ebb4cb722e329ba4a11/0124638821v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/09/6c/096c74cd493fabd9824c30e3507605c4/0128861312v2.jpeg)