Neurodegenerative Erkrankungen Wie wird der zelluläre Müll abgebaut?
Viele neurodegenerative Erkrankungen wie Alzheimer, Parkinson und Chorea Huntington gehen mit der Ansammlung von anormalen und verklumpten Proteinen einher. Zellulärer „Müll“ dieser Art kann in zellulären Recyclingstationen beseitigt werden – in den so genannten Lysosomen. Wissenschaftler am Max-Planck-Institut für Biochemie in Martinsried bei München haben jetzt eine neue Familie von Helferproteinen entdeckt, die markierten Proteinmüll erkennen und zu den Lysosomen geleiten, wo er dann zerlegt und recycelt wird.
Anbieter zum Thema
Martinsried – Proteine, die Komponenten unseres Körpers, die den Großteil der Funktionen in unseren Zellen ausführen, steuern oder organisieren – sind aus Ketten von aneinandergereihten Aminosäuren aufgebaut. Entsprechend ihrer Funktion werden sie wie bei einem Origami in spezifische und komplexe dreidimensionale Strukturen gefaltet. Da Proteinfaltung und Erhaltung dieser Strukturen höchst störanfällig sind, können Proteine falsch gefaltet werden oder sogar Klumpen (Aggregate) bilden. Solch unerwünschter Proteinmüll kann in Zellen toxisch wirken und sogar zum Zelltod führen. Viele neurodegenerative Krankheiten sind dadurch charakterisiert, dass in neuronalen Zellen von entsprechenden Patienten falsch gefaltete Proteine oder Aggregate akkumulieren. Um neue Strategien für eine mögliche Prävention oder Heilung dieser Krankheiten entwickeln zu können, ist es notwendig, genau zu verstehen, wie Zellen ihren toxischen Müll entsorgen.
Bäckerhefe als Modellorgansimus
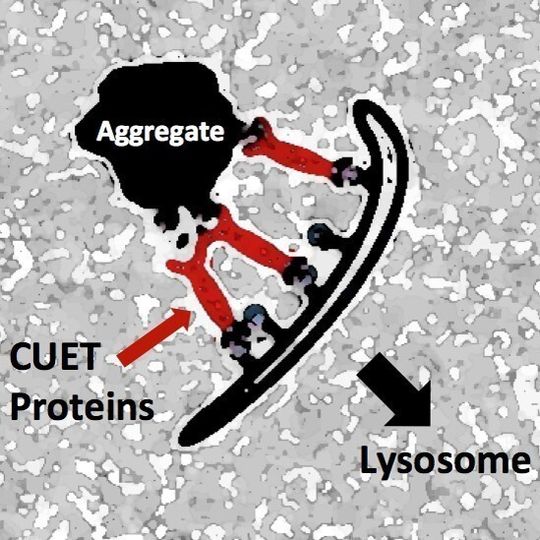
Wissenschaftler aus dem Labor von Stefan Jentsch am Max-Planck Institut für Biochemie haben jetzt erfolgreich die Bäckerhefe eingesetzt, um neue Müllentsorgungswege zu entdecken. Kefeng Lu, ein Wissenschaftler der Arbeitsgruppe, hat eine neue Klasse von Helferproteinen (CUET-Proteine) entdeckt, die in der Hefe und im Menschen vorkommen und zellulären Müll erkennen, der mit dem Proteinetikett Ubiquitin markiert ist. Diese neu entdeckten Helferproteine geleiten den zellulären Abfall durch einen bestimmten Transportweg namens Autophagozytose (wörtlich „sich selbst verdauen“) zu den Lysosomen. Die Max-Planck-Forscher konnten auch zeigen, dass ein toxisches Protein, das der abnormalen Form des Proteins Huntingtin der Chorea Huntington-Patienten sehr ähnlich ist, durch den neu entdeckten Abbauweg effektiv entsorgt wird. Der Abbauweg ist für aggregat-bildende Proteine wie Huntingtin anscheinend hochspezifisch und scheint sogar effektiver als zuvor beschriebene Mechanismen zu sein.
Neue Möglichkeiten für die Bekämpfung neurodgenerativer Krankheiten
Da der neu gefundene Abbauweg auch in der Hefe aktiv ist, wollen die Forscher jetzt die experimentellen Möglichkeiten dieses Modellorganismus‘ voll ausschöpfen, um den Mechanismus weiter zu untersuchen. Eine detaillierte Analyse ist entscheidend, um zu verstehen, wie Proteinverklumpungen zu Erkrankungen führen und um neue Konzepte zur Vorbeugung zu entwickeln.
Originalpublikation: K. Lu, I. Psakhye and S. Jentsch; Autophagic clearance of polyQ proteins mediated by the conserved CUET protein family; Cell, July 17, 2014. DOI: 10.1016/j.cell.2014.05.048
(ID:42828685)






:quality(80)/p7i.vogel.de/wcms/75/6d/756dd7e64300810ccc230806aca56bce/0131180204v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/52/1d/521df5ca6deda3d908cbe03b9da19bfa/0129719159v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/3e/5a/3e5a8bb1ee710df312860e851e510230/0131073124v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d5/b1/d5b145d1d1c81f059eca6f7b8a54fa35/0130471995v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0130924147v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a6/e0/a6e0ab14cf7f6b22d536f6ca6e5fb777/0130793394v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/3d/c2/3dc269b3435d97799061920f4a281393/0131172010v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/0b/ae/0bae37390a1d66dbbdf9a795e677f45a/0131115837v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/27/10/27106c0034e605f1f34d8c2caafae058/0131092893v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/81/64/8164cf2ffcd70252fb956edf385c5294/0131082949v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fe/3e/fe3e220cf6ac0f453fc75187c04572fd/0130535166v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/e2/5e/e25e2c9f40617e17d32524787c6ece1d/0130248690v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/2e/17/2e1795b6750cc3eaad6ba81c0bc79d16/0100811496v7.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/27600/27667/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/6400/6447/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/69/5b/695b8e4976caa/40jahre-denios-logo-srgb-web.svg)
:quality(80)/p7i.vogel.de/wcms/e9/a7/e9a7830ab3e8457a7bbf4522cebdbcf7/0126714724v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/7c/437c11c55c00cd1a1691578177be09cd/0127190431v1.jpeg)