Adsorptionsprozesse Die Stachelschwein-Allegorie in der Chemie – experimentell bestätigt
Die chemisch-physikalischen Prozesse bei der Adsorption an Oberflächen sind schon relativ gut verstanden. Nun hat ein Physiker-Team der Universität Regensburg erstmals direkt gemessen, wie ein Kohlenstoffmonoxid-Atom bei der Annäherung an ein Eisenatom von der schwachen Physisorption in die starke Chemisorption übergeht. Was das mit Stachelschweinen zu tun hat, lesen Sie im Folgenden.
Anbieter zum Thema
Regensburg – Der Philosoph Arthur Schopenhauer hat mit seiner Stachelschwein-Allegorie ein Gleichnis entwickelt, welches einen gewissen Wohlfühlabstand zwischen Menschen erklärt. Demnach fühlen sich Menschen bei zu großem Abstand allein und bei zu kleinem Abstand unwohl aufgrund abstoßender Charaktereigenschaften. Den optimalen Abstand hat er anhand der Stachelschweine so erklärt: „An einem kalten Tag entwickelt eine Gruppe Stachelschweine ein allen gemeines Wärmebedürfnis. Um es zu befriedigen, suchen sie die gegenseitige Nähe. Doch je näher sie aneinanderrücken, desto stärker schmerzen die Stacheln der Nachbarn. Da aber das Auseinanderrücken wieder mit Frieren verbunden ist, verändern sie ihren Abstand, bis sie die erträglichste Entfernung gefunden haben.“
Der Physiker und Nobelpreisträger Richard Feynman beschreibt in seinem dreibändigen Lehrbuch „The Feynman Lectures on Physics“ gleich im ersten Kapitel ein ähnliches Phänomen beim Verhalten der elementaren Bausteine der Materie, den Atomen. „… alle Dinge bestehen aus Atomen – kleine Teilchen die ständig in Bewegung sind, sich anziehen, wenn sie etwas entfernt sind voneinander, sich aber abstoßen, wenn man sie aufeinander drückt“. Dies bringt die Wechselwirkung zwischen Atomen stark vereinfacht auf den Punkt.
Zwei „Wohlfühlabstände“
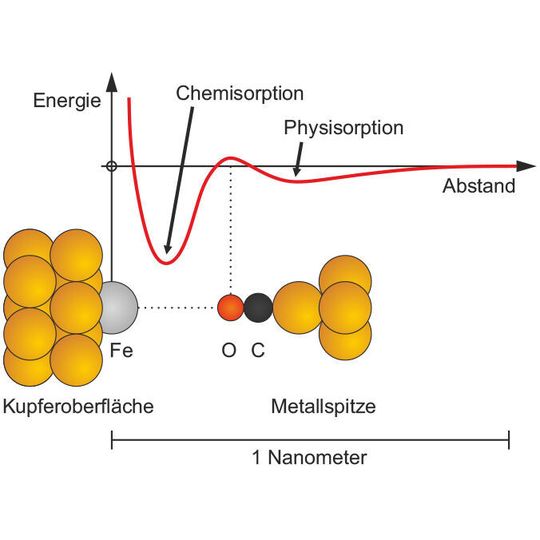
In der Realität ist es jedoch wie so oft etwas komplizierter. So hat der Physiker John Lennard-Jones bereits 1932 eine wichtige Komplikation für die Natur der Atombindungen festgestellt. Es können nämlich gleich zwei Bindungstypen mit verschiedenen Gleichgewichtsabständen existieren: eine schwache Bindung mit größerem Gleichgewichtsabstand, genannt Physisorption und eine starke chemische Bindung mit kurzem Gleichgewichtsabstand, die Chemisorption.
Physisorption ist beispielsweise für die Anhaftung von Staub auf Oberflächen oder von Geckos auf Wänden verantwortlich, sie ist also relativ leicht zu überwinden. Die Chemiesorption hingegen ist zehn bis hundert Mal stärker als die Physisorption und eine „echte“ chemische Bindung, bei der sich die adsorbierten Moleküle und die Substratoberfläche chemisch verändern.
Das Wechselspiel der beiden Adsorptionsarten ist wichtig für den Ablauf chemischer Reaktionen auf Oberflächen, zum Beispiel bei der Abgasreinigung im Autokatalysator oder bei der katalytischen Gewinnung chemischer Grundstoffe. Die zwei Adsorptionsarten werden durch zwei Minima in einer Energiekurve dargestellt (s. Grafik). Derartige Grafiken werden seit Jahrzehnten in den Lehrbüchern der physikalischen Chemie und Oberflächenphysik abgedruckt, dabei waren sie bisher nur theoretisch postuliert.
![Abb.1: Bei der Stickstoff-Adsorption bei 77 K [5] ist der Platzbedarf von der Adsorptions-Position des Moleküls abhängig, anders als bei Argon und Krypton, bei denen sich jeweils nur eine Position ergibt (Ausschnitt). (3P) Abb.1: Bei der Stickstoff-Adsorption bei 77 K [5] ist der Platzbedarf von der Adsorptions-Position des Moleküls abhängig, anders als bei Argon und Krypton, bei denen sich jeweils nur eine Position ergibt (Ausschnitt). (3P)](https://cdn1.vogel.de/v_8c7l0yAxUzX-irhoM266JfrnU=/320x180/smart/filters:format(jpg):quality(80)/images.vogel.de/vogelonline/bdb/1598700/1598735/original.jpg)
Spezifische Oberflächen verlässlich bestimmen
Ist die BET-Methode zu oberflächlich?
Kontrollierte Annäherung von Atomen
Einer Gruppe experimenteller Physiker von der Universität Regensburg ist es nun erstmals gelungen, den Übergang von der Physisorption in die Chemisorption direkt zu messen. Möglich machte dies eine Versuchsanordnung in der Rasterkraftmikroskopie. Die Wissenschaftler befestigten dazu ein Kohlenstoffmonoxid-Molekül an der Spitze ihres Rasterkraftmikroskops und näherten es dann an ein einzelnes Eisenatom auf einer Kupferoberfläche an. Dabei zeichneten sie die Kraftentwicklung bei der Annäherung auf.
Unterstützt wurden die Experimentalphysiker von einem Team von Quantenchemikern der Ludwig-Maximilians-Universität München, welche die theoretische Erklärung für den Versuch beisteuerten. So muss beim Übergang von der Physisorption zur Chemisorption zunächst eine Potentialbarriere überwunden werden. Dies erfolgt mit einem Prozess der Hybridisierung, den die Chemiker mit ihren quantenmechanischen Rechnungen erklärt und nachgewiesen haben.
Originalpublikation: Ferdinand Huber, Julian Berwanger, Svitlana Polesya, Sergiy Mankovsky, Hubert Ebert, Franz J. Giessibl: Chemical bond formation showing a transition from physisorption to chemisorption, Science 12. Sep 2019; DOI: 10.1126/science.aay3444
(ID:46137427)






:quality(80)/p7i.vogel.de/wcms/c9/16/c9162be8c6014187286dda23e57f8793/0130654555v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/9f/9d/9f9d6fc46606d654deca536f05102f7a/0130752952v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/58/bb58da17d7bb11b44fcae8d06c35df76/0130791510v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/0f/0c/0f0c5774037cc09a3536d24702f6204b/0130936383v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0130924147v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a6/e0/a6e0ab14cf7f6b22d536f6ca6e5fb777/0130793394v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/63/85/638523e67603079a004bbd3a99b6ad92/0130856502v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/df/3d/df3d3f7d7b425eabae87bab4ef68bd6c/0130259765v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/b9/32/b9326aa0b6f26d5e5eeee82c86aab8b6/0130976290v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/2d/5f/2d5f14d92ec22f38682c6d240600579f/0131000090v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/19/40/194054b15f3c0e161583d7ea8917ec3f/0130974372v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/e2/5e/e25e2c9f40617e17d32524787c6ece1d/0130248690v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/09/88/09883aaf7db3151a2e894d56c2a515d4/0130982666v2.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/69/67/696769fab6999/kern-logo2023-blau-4c-or.png)
:fill(fff,0)/p7i.vogel.de/companies/68/87/688727a5ba8d5/logo-dr-weigert--de-hygiene-mit-system-200-.png)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/86900/86921/65.jpg)
:quality(80)/p7i.vogel.de/wcms/48/02/4802e79803f53d71782241e6ec88eb92/0125813301v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/c8/ff/c8ffe0dbfa8e6a0c2f351334f9bc3c96/0129177583v2.jpeg)