Polymeranalyse Neue Spektroskopiemethode charakterisiert Polymere und Bionanopartikel
Die Komplexität der Polymeranalytik nimmt ständig zu und damit die Anforderungen an die Analysenmethoden. Eine neue elektrophoretische Mobilitäts-basierte Methode erlaubt die schnelle, unabhängige Analyse über einen weiten Nanometerpartikelbereich.
Anbieter zum Thema
In der modernen Analytik von natürlichen und synthetischen Polymeren spielen die Größen- und Molekulargewichtsbestimmung sowie die Molekulargewichtsverteilung eine entscheidende Rolle, denn die physikochemischen und werkstofftechnischen Eigenschaften der Polymere sind eng hiermit verbunden. Dies gilt nicht nur in der Forschung, sondern auch in der Entwicklung und Produktion. Es gibt eine breite Palette von relativ einfachen bis zu hochkomplexen Analysenmethoden, um Polymere in ihren verschiedensten Aggregatzuständen zu charakterisieren. Zu den einfacheren Methoden gehören u.a. die Titration um End-Gruppen zu bestimmen oder die Größenauschlusschromatographie (SEC, size exclusion chromatography). Komplexe Analysemethoden sind beispielsweise die zweidimensionale NMR-Spektroskopie (NMR, nuclear magnetic resonance), die Kleinwinkellaserlichtstreuung (LALL) oder die MALDI-Tandemmassenspektrometrie (MALDI, matrix-assisted laser desorption/ionization).
Sowohl natürlich vorkommende Polymere wie Dextrane, Stärke oder Pullolane als auch voll- oder teilsynthetische Polymere wie Polystyrole werden mit immer größeren Molekulargewichten und Partikelgrößen hergestellt und isoliert. Daraus ergeben sich auch immer höhere Anforderungen an die Analysenmethoden, um das zahlenmäßig gemittelte oder gewichtsgemittelte Molekulargewicht derartiger ultrahochmolekularer Polymere zu bestimmen. Ähnlich stellt sich die Situation bei der Größenbestimmung von Polymerpartikeln dar, denn polymerbasierende Nanopartikel sind im Bereich der Material- und Biowissenschaften zunehmend von entscheidender Bedeutung. In vielen Fällen spielt bei der Anwendung in F&E und Qualitätskontrolle die Sensitivität der Methode, deren Schnelligkeit die gewünschten Daten zu liefern sowie die Selektivität eine wesentliche Rolle. Hinzu kommt die Komplexität der Technik oder anders gesagt, deren Robustheit, und ob Referenzmaterialien benötigt werden.
In den letzten Jahren konnte nun eine neue Analysenmethode entwickelt werden, die besonders für den Bereich von 2,5 bis 150 nm Nanoteilchendurchmesser geeignet ist. Diese eigentlich aus der Aerosolphysik stammende Methode basiert auf Nanoelektrospray gekoppelt mit einem differentiellen Mobilitätsanalysator (DMA) und einem Kondesationsteilchendetektor (CPC) [1, 2, 3]. Bei dem DMA handelt es sich um eine Trenntechnik die zur großen Gruppe der Ionenmobilitätsanalysatoren gehört und in dieser Ausformung bei Atmosphärendruck arbeitet.
GEMMA – die Methode
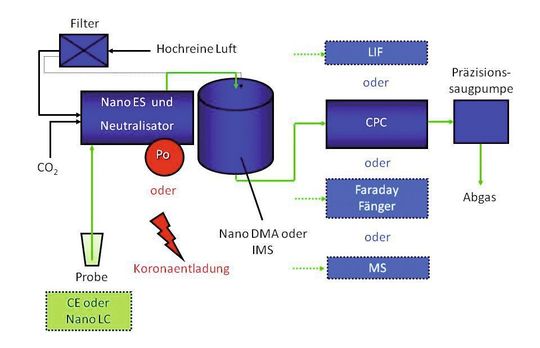
Die in der Literatur als GEMMA (gas-phase electrophoretic mobility molecular analyzer), macro-IMS (Macroion Mobility Spectrometer) oder SMPS (Scanning Mobility Particle Sizing) bezeichnete Methode verwendet das Polymer vorzugsweise in gelöster Form oder als Suspension, Emulsion oder Gel, wobei wässrige Lösungsmittelsysteme nötig sind. Die Probe wird über eine Fused-Silika-Kapillare in eine Nanoelektrosprayquelle eingebracht, unterstützt durch eine angelegte Spannung im kV-Bereich und durch einen Strom von CO2 und partikelfreier Luft (s. Abb. 1). Ein direkte Kopplung mit einer CE oder Nano-LC, mit denen eine Vortrennung nach orthogonalen Trennprinzipien durchgeführt werden kann, ist hier möglich. Es wird im so genannten Taylor- cone-jet-Modus gearbeitet. Dabei wird eine entsprechend niedrige Konzentration eingesetzt, sodass nur ein Nanopartikel oder Molekül pro gebildetem Aerosoltröpfchen (ca. 160 nm Durchmesser) vorliegt und die Aerosoltröpfchen den Taylorkonus am Ende der Spraykapillare so verlassen als wären sie in einer Perlenkette aneinandergereiht. Diese Nanoaerosoltröpfchen werden nun durch den laminaren Fluss der beiden Gase in einen Neutralisator gebracht, wobei die mehrfach geladenen Aerosoltröpfchen dabei bereits einen wesentlichen Teil der neutralen Lösungsmittelmoleküle verlieren und in ein Ladungsgleichgewicht gebracht werden.
(ID:27354870)






:quality(80)/p7i.vogel.de/wcms/f4/d9/f4d915245e41f3f0271e2e640063f422/0130738781v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/75/6d/756dd7e64300810ccc230806aca56bce/0131180204v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/52/1d/521df5ca6deda3d908cbe03b9da19bfa/0129719159v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/3e/5a/3e5a8bb1ee710df312860e851e510230/0131073124v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0130924147v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a6/e0/a6e0ab14cf7f6b22d536f6ca6e5fb777/0130793394v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/3d/c2/3dc269b3435d97799061920f4a281393/0131172010v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/0b/ae/0bae37390a1d66dbbdf9a795e677f45a/0131115837v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/27/10/27106c0034e605f1f34d8c2caafae058/0131092893v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/81/64/8164cf2ffcd70252fb956edf385c5294/0131082949v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fe/3e/fe3e220cf6ac0f453fc75187c04572fd/0130535166v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/e2/5e/e25e2c9f40617e17d32524787c6ece1d/0130248690v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/2e/17/2e1795b6750cc3eaad6ba81c0bc79d16/0100811496v7.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/69/67/696769fab6999/kern-logo2023-blau-4c-or.png)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/20500/20552/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/60/dd/60ddc39947ebf/brand-logo-registered.png)
:quality(80)/p7i.vogel.de/wcms/c8/ff/c8ffe0dbfa8e6a0c2f351334f9bc3c96/0129177583v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/da/8c/da8cf22ae4626f0fcc005babf1717a15/0125712849v2.jpeg)