Mikroskopie Neues Verfahren verbessert Beobachtung von Proteinen unter dem Mikroskop
Forscher der Goethe-Universität in Frankfurt haben ein neues Verfahren entwickelt, dass die Beobachtung von Proteinen unter dem Mikroskop verbessert. Die Proteine werden dabei mit einer leuchtenden Miniatursonden fusioniert. Die so erreichte hochauflösende Mikroskopie basiert auf dem Schlüssel-Schloß-Prinzip.
Anbieter zum Thema
Frankfurt – Um Proteine im Mikroskop sichtbar zu machen, werden sie meist auf DNA-Ebene mit fluoreszierenden Proteinen fusioniert. Allerdings sind diese leuchtenden Marker relativ groß, so dass sie die Funktion der Proteine beeinträchtigen können. Außerdem sind sie aufgrund ihrer Größe oft weit vom zu beobachtenden Protein entfernt.
Das gleiche Problem tritt bei der ebenfalls weit verbreiteten Markierung mittels Antikörpern auf. Auch hier kann die große Distanz zwischen Protein und Sonde zu fehlerhaften Beobachtungen führen. Um dieses Problem zu umgehen, haben Wissenschaftler der Goethe-Universität in Frankfurt nun sehr kleine Markierungssonden für die hochauflösende Mikroskopie entwickelt.
Entwickler setzten auf Schlüssel-Schloss-Prinzip
Die hochauflösende Methode basiert auf dem Schlüssel-Schloss-Prinzip: Dazu wird das zu beobachtende Protein mit einer sehr kleinen Sonde, einem Histidin-Tag, fusioniert. An diesen bindet spezifisch das fluoreszenzmarkierte Molekül tris Nitrilotriessigsäure (trisNTA). Da beide Teile der Sonde extrem klein sind, rückt die fluoreszierende Markierung sehr nahe an das Protein. Die Entfernung beträgt nur zwei Nanometer, was rund zehnmal näher ist als bei konventioneller Antikörpermarkierung.
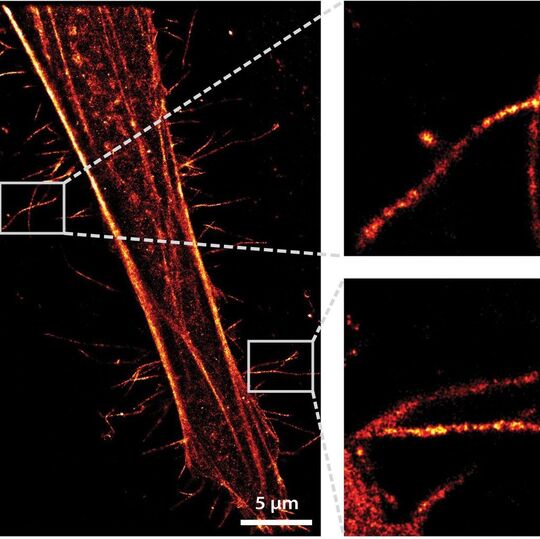
Die auf den Namen SLAP („Small LAbeling Pair“) getaufte Technik wurde in enger Zusammenarbeit zwischen den Gruppen um die Professoren Mike Heilemann (Institut für Physikalische und Theoretische Chemie) und Robert Tampé (Institut für Biochemie) an der Goethe-Universität entwickelt und in hochauflösender Fluoreszenz-Mikroskopie angewendet. Mit dieser Technik, die 2014 mit dem Nobelpreis für Chemie honoriert wurde, kann man - dank der trickreichen Umgehung der bisherigen Auflösungsgrenze - einzelne Proteine und Moleküle sichtbar machen. So konnten beispielsweise mit SLAP markierte Bestandteile des Zellskeletts mit einer Auflösung von 40 nm dargestellt werden.
Vorteil der Methode
„Der große Vorteil dieser Methode zeigte sich bei der Markierung von Komponenten der Antigen-Prozessierung“, erläutert Tampé. Diese essentielle Maschinerie des adaptiven Immunsystems sorgt dafür, dass Fragmente von Erregern, etwa Viren, auf der Zelloberfläche präsentiert werden. Dadurch werden infizierte Zellen vom Immunsystem als solche erkannt und eliminiert. Dank der neuen SLAP-Markierungsmethode kombiniert mit der hochauflösenden Mikroskopie konnte die Größe dieser Proteinkomplexe nun auf etwa 50 nm eingegrenzt werden.
„Jetzt wissen wir, dass der gleiche Komplex durch die konventionelle Markierung mit Antikörpern künstlich vergrößert dargestellt wurde“, fügt Heilemann hinzu. Da die SLAP-Markierungsmethode leicht anwendbar ist, sind die Frankfurter Forscher überzeugt, damit auch auf längere Sicht einen Beitrag zur genaueren Darstellung von krankheitsrelevanten zellulären Prozessen geleistet zu haben.
(ID:43589963)






:quality(80)/p7i.vogel.de/wcms/75/6d/756dd7e64300810ccc230806aca56bce/0131180204v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/52/1d/521df5ca6deda3d908cbe03b9da19bfa/0129719159v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/3e/5a/3e5a8bb1ee710df312860e851e510230/0131073124v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/d5/b1/d5b145d1d1c81f059eca6f7b8a54fa35/0130471995v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/9a/a89a4fd1c2742eb96d85ff270e9f52d4/0131047740v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0130924147v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a6/e0/a6e0ab14cf7f6b22d536f6ca6e5fb777/0130793394v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/3d/c2/3dc269b3435d97799061920f4a281393/0131172010v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/0b/ae/0bae37390a1d66dbbdf9a795e677f45a/0131115837v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/27/10/27106c0034e605f1f34d8c2caafae058/0131092893v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/81/64/8164cf2ffcd70252fb956edf385c5294/0131082949v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/e9/bbe97af9120730250441d33706d76f2a/0131122618v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3c/0f/3c0f1dc6670ceea51950c2b0fc339173/0131057362v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fe/3e/fe3e220cf6ac0f453fc75187c04572fd/0130535166v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/e2/5e/e25e2c9f40617e17d32524787c6ece1d/0130248690v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/2e/17/2e1795b6750cc3eaad6ba81c0bc79d16/0100811496v7.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/69/67/696769fab6999/kern-logo2023-blau-4c-or.png)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/76800/76895/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/68/07/6807ad98568ce/logo-elementar-rgb.jpeg)
:quality(80)/p7i.vogel.de/wcms/10/53/10531cb8757c536d4d3ea325e082f5f4/0128840645v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/b1/7a/b17a1957b45bcc9acbba24ec709f824c/0126987477v3.jpeg)