Automatisierte Mikroskopie & Wirkstoffforschung Weniger „Fallen Angels": Mit Maschinellem Lernen schneller zum Wirkstoff
Die Suche nach neuen Wirkstoffen ist ein langwieriger und teurer Prozess. Ihn zu beschleunigen und kostengünstiger zu machen, käme nicht nur Patienten zugute, sondern wäre nicht zuletzt auch ökonomisch enorm sinnvoll. Genau das wollen Heidelberger Forscher nun erreichen: Mit Hilfe einer neu entwickelten Software, automatisierter Mikroskopie sowie deren Verknüpfung mit Künstlicher Intelligenz (KI) und Maschinellem Lernen.
Anbieter zum Thema
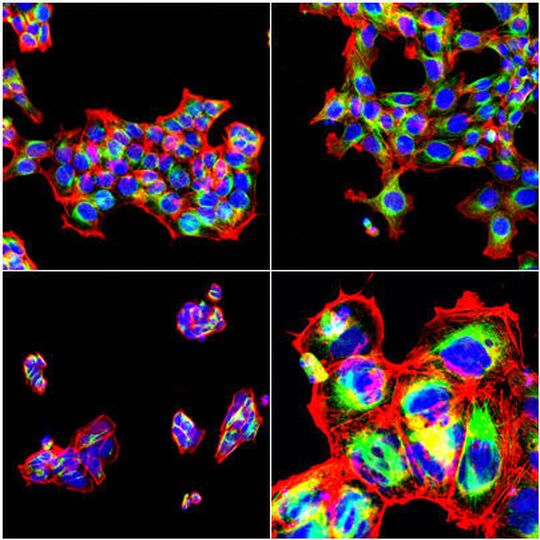
Heidelberg – Die Entwicklung neuer Medikamente ist ein langwieriger, teurer Prozess. Oft stellt sich erst nach langer Entwicklungszeit heraus, dass ein potentieller neuer Wirkstoff unerwünschte Nebenwirkungen verursacht und damit aufgegeben werden muss. Das treibt die Kosten zusätzlich in die Höhe. Bei der Suche nach neuen Wirkstoffen werden meist tausende von Substanzen parallel getestet, dabei wird jedoch nur ein sehr kleiner Ausschnitt ihrer biologischen Aktivität erfasst. Diese enge Charakterisierung neuer Wirkstoffe kann dazu führen, dass unerkannte Wirkmechanismen übersehen werden, die bei der Behandlung anderer Krankheiten helfen könnten.
Neue Medikamente kostengünstiger und schneller entwickeln mit Hilfe von bildbasierten Analysen – dafür vergibt der Europäische Forschungsrat ERC nun erstmals einen „Proof-of-Concept-Grant" an Wissenschaftler vom Deutschen Krebsforschungszentrum und der Universität Heidelberg.
Präklinik: Wirkstoffkandidaten früh umfassend charakterisieren
„Es wäre wünschenswert und vor allem ökonomisch sinnvoll, neue Wirkstoffkandidaten gleich während der frühen präklinischen Entwicklung umfassend zu charakterisieren", sagt Michael Boutros vom Deutschen Krebsforschungszentrum (DKFZ) und von der Medizinischen Fakultät Mannheim der Universität Heidelberg. Sein Projekt „Rematch - Image-based Analysis for Drug Discovery and Repurposing", das vom Europäischen Forschungsrat (ERC) nun als „Proof of Concept" finanziell gefördert wird, setzt genau hier an. Mit diesem Förderinstrument unterstützt der Forschungsrat Wissenschaftler dabei, das wirtschaftliche Potenzial ihrer in einem laufenden ERC-Förderprojekt entwickelten Ergebnisse oder Technologien weiterzuentwickeln, um sie zum Beispiel in Ausgründungen umzusetzen.
Software für bildbasierte Screenings per automatisierter Mikroskopie
Die Idee zu Rematch ging aus Boutros' ERC-Projekt „Syngene" hervor. Es basiert auf einer in seiner Abteilung entwickelten Software für bildbasierte Screenings, die es erlaubt, eine Vielzahl an Reaktionen von Zellen auf Wirkstoffe sehr breit und kostengünstig zu erfassen und mit Verfahren des maschinellen Lernens zu analysieren.
Dafür reicht es aus, die Veränderungen von nur einer Handvoll zellulärer Strukturen zu beobachten. „Jede Testsubstanz bewirkt subtile Veränderungen in der Struktur und Verteilung dieser Biomoleküle, die mit Fluoreszenzfärbungen sichtbar gemacht und durch automatisierte Mikroskopie dokumentiert werden. Zusammengenommen ergibt sich so ein umfassendes Bild vom Zustand der Zelle", erklärt Boutros das Prinzip.
Weniger „Fallen Angels“ – per KI und maschinellem Lernen
Um jedoch die biologische Aussage eines solchen Bildes interpretieren zu können, muss den Anwendern der Methode eine Referenz zur Verfügung stehen. Mit Rematch wollen die Forscher um Boutros nun eine Referenzdatenbank für solche Wirkstoff-Muster erstellen. Dabei verwenden sie neue Ansätze der künstlichen Intelligenz und des maschinellen Lernens.
:quality(80)/images.vogel.de/vogelonline/bdb/1330100/1330148/original.jpg)
Biomarker-Konstellationen bei MS
Multiple Sklerose: Wie NMR und Machine Learning die Diagnostik verbessern können
Die sehr großen Datensätze der Referenzdatenbank dienen dazu, den Effekt einer Testsubstanz mit dem von bereits zugelassenen oder gescheiterten Wirkstoffen – so genannten „Fallen Angels" – abzugleichen, um Nebenwirkungen frühzeitig auszuschließen und neue Wirkungsfelder zu erkunden. Die ERC-Förderung ermöglicht es Boutros nun, das wirtschaftliche Potential der von seiner Abteilung neu entwickelten analytischen Ansätze und Software-Lösungen sowie die Möglichkeit einer Ausgründung des Projekts zu prüfen und anzustoßen.
* Dr. S. Kohlstädt: Deutsches Krebsforschungszentrum (DKFZ), 69120 Heidelberg
(ID:45541151)






:quality(80)/p7i.vogel.de/wcms/fe/3e/fe3e220cf6ac0f453fc75187c04572fd/0130535166v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/de/74/de74b5de1a05065fd65e37f9818b0154/0130573678v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/46/10/46104916e8a69933218fded0d5925feb/0130443323v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c9/16/c9162be8c6014187286dda23e57f8793/0130654555v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0130924147v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a6/e0/a6e0ab14cf7f6b22d536f6ca6e5fb777/0130793394v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/63/85/638523e67603079a004bbd3a99b6ad92/0130856502v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/df/3d/df3d3f7d7b425eabae87bab4ef68bd6c/0130259765v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/b9/32/b9326aa0b6f26d5e5eeee82c86aab8b6/0130976290v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/2d/5f/2d5f14d92ec22f38682c6d240600579f/0131000090v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/19/40/194054b15f3c0e161583d7ea8917ec3f/0130974372v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/e2/5e/e25e2c9f40617e17d32524787c6ece1d/0130248690v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/09/88/09883aaf7db3151a2e894d56c2a515d4/0130982666v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/94/ea/94ea0a6bc66aa9796ba99895d0840e18/0131032415v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ea/fc/eafc19c5d59b25706790fe14f814eb88/0131009351v3.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/115900/115965/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/68/87/688727a5ba8d5/logo-dr-weigert--de-hygiene-mit-system-200-.png)
:fill(fff,0)/p7i.vogel.de/companies/62/06/62066242d6e45/kup-logo.jpeg)
:quality(80)/p7i.vogel.de/wcms/88/75/887510bba40cd65b5b70487a7b1114d8/0127966319v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/b1/7a/b17a1957b45bcc9acbba24ec709f824c/0126987477v3.jpeg)