Ionenaustauschchromatographie Ladungsvarianten von Biopharmazeutika sicher charakterisieren
Biotherapeutische Proteine wie monoklonale Antikörper (mAbs) sind heterogen und kommen als Gemisch von Molekülvarianten mit ähnlicher Struktur vor. Die Heterogenität von mAbs lässt sich z.B. mit der Ionenaustauschchromatographie erkennen. Änderungen des Ladungscharakters können sich signifikant auf Struktur, Stabilität, Bindungsaffinität und Wirksamkeit der Biopharmazeutika auswirken.
Anbieter zum Thema
Therapeutische Proteine wie monoklonale Antikörper (mAbs) sind außerordentlich komplex und erfordern zur Überprüfung ihrer Struktur eine Vielzahl physikalisch-chemischer Tests. Ist die Struktur erst einmal validiert, muss sie von der Entwicklung über die Herstellung bis zur Vermarktung kontinuierlich überwacht werden, um die Sicherheit und Wirksamkeit des Medikaments zu gewährleisten. Regulatorische Richtlinien wie ICH Q6B konzentrieren sich auf die Analyse der Kernstruktur und der physikalisch-chemischen Eigenschaften, die für die Hersteller der Präparate erforderlich sind, um die wie ein Fingerabdruck unverwechselbare strukturelle Gleichartigkeit ihres Kandidatenmoleküls bei der Klonselektion, Prozessentwicklung und letztlich für die Stabilität des produzierten Medikaments nachzuweisen. Als kritische Qualitätsattribute (Critical Quality Attributes, CQAs) der Moleküle gelten Eigenschaften, die ihre klinische Sicherheit oder Wirksamkeit betreffen. CQAs werden mithilfe von Analysen kontrolliert, die dazu dienen, die Variabilität zwischen den einzelnen Chargen zu minimieren. Hierzu gehören u.a.:
- Ladungsvarianten-Charakterisierung,
- Aggregatanalyse,
- Glycan-Analyse,
- intakte Massenanalyse und
- Peptid-Mapping.
Ladungsheterogenität von Proteinen – warum so wichtig?
Ladungsvarianten können in therapeutischen Proteinprodukten aus vielerlei Gründen auftreten, einschließlich Sequenzänderungen, posttranslationaler Modifizierung und chemischer Abbauvorgänge. Die häufigsten Ursachen von Ladungsvarianten sind Deamidierung, Isomerisierung, Succinimid-Bildung, Oxidation, Sialinsäurebildung, Pyroglutamat-Bildung am N-Terminus, C-terminale Lysin-Abspaltung und Aggregation. Je nach Art der Modifizierung kann die sich ergebende Spezies saurer oder basischer als das mAbs-Hauptmonomer sein. Da diese Änderungen die Stabilität und biologische Aktivität des Produkts beeinflussen können, stellt Ladungsheterogenität eine Herausforderung für den Nachweis der Vergleichbarkeit dar.
Für potenziell innovative Biologika oder Biosimilars müssen jegliche Abweichungen zügig identifiziert und so frühzeitig wie möglich minimiert werden. Zu den Prozessmaßnahmen können die weitere Optimierung der Zellkulturbedingungen oder die Weiterentwicklung der Formulierungen gehören.
Ein schnelles und sicheres Programm zur Charakterisierung von Ladungsvarianten kann die Kandidaten-Entwicklung beschleunigen und Strategien zur effizienten, kontinuierlichen Kontrolle unterstützen.
Therapeutische Ladungsvarianten trennen
Ionenaustauschchromatographie (IEC) wird weithin als der Goldstandard für die Analyse von Biomolekülen genutzt und bleibt weiterhin eine Schlüsseltechnologie für die Ladungsvariantenanalyse. Bei der Ionenaustauschchromatographie werden Moleküle anhand von Ionengruppen auf der Proteinoberfläche getrennt, die sich in elektrostatischer Wechselwirkung mit entgegengesetzt aufgeladenen Ionengruppen an der Oberfläche der stationären Phase befinden:
- Als Anionenaustauscher eingesetzte Säulen verfügen über eine positiv geladene stationäre Phase und werden oberhalb des isoelektrischen Punkts (Isoelectric Point, PI) des Proteins betrieben.
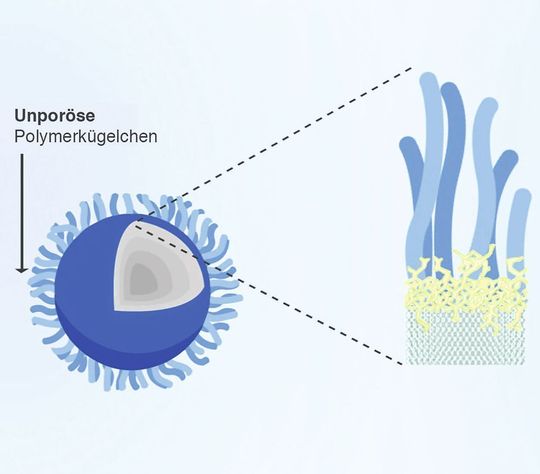
- Als Kationenaustauscher eingesetzte Säulen enthalten negativ geladene Gruppen, die auf eine stationäre Phase in Polymerform gepfropft werden (s. Abb. 1). Sie werden bei pH-Werten betrieben, die unterhalb des PI des Proteins liegen. Kationenaustauschchromatographie wird gewöhnlich für die Analyse von monoklonalen Antikörpern (mAbs) eingesetzt, da hier aufgrund des hohen Anteils an basischen Rückständen der Einsatz von basischer Oberflächenchemie angeraten ist. Saure Varianten werden von der stationären Phase in geringerem Maße zurückgehalten und zuerst eluiert; ihnen folgen die neutralen und schließlich die basischen Varianten (s. Abb. 2).
Viele der häufig verwendeten Chromatographieverfahren wie die Umkehrphasen-Chromatographie (Reverse Phase, RP), arbeiten mit organischen Lösungsmittel, die das Zielprotein denaturieren oder entfalten und es von seinem eigentlichen nativen Zustand entfernen. Ein Vorteil der Ionenaustauschchromatographie besteht darin, dass es bei der Trennung nicht zu einer Denaturierung kommt. Die Elution erfolgt unter Verwendung eines Salz- oder pH-Gradienten, um die elektrostatischen Wechselwirkungen zwischen dem Protein und der stationären Phase zu unterbrechen.
(ID:44980372)






:quality(80)/p7i.vogel.de/wcms/c9/16/c9162be8c6014187286dda23e57f8793/0130654555v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/9f/9d/9f9d6fc46606d654deca536f05102f7a/0130752952v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bb/58/bb58da17d7bb11b44fcae8d06c35df76/0130791510v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/0f/0c/0f0c5774037cc09a3536d24702f6204b/0130936383v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/7b/dc7b0f7209d2dedf548b5019da2e1b9c/0130556742v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0130924147v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a6/e0/a6e0ab14cf7f6b22d536f6ca6e5fb777/0130793394v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/63/85/638523e67603079a004bbd3a99b6ad92/0130856502v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/df/3d/df3d3f7d7b425eabae87bab4ef68bd6c/0130259765v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/b9/32/b9326aa0b6f26d5e5eeee82c86aab8b6/0130976290v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/2d/5f/2d5f14d92ec22f38682c6d240600579f/0131000090v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/19/40/194054b15f3c0e161583d7ea8917ec3f/0130974372v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/e2/5e/e25e2c9f40617e17d32524787c6ece1d/0130248690v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/09/88/09883aaf7db3151a2e894d56c2a515d4/0130982666v2.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/76800/76895/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/8800/8870/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/69/2e/692ed0d59df43/a1sciences-4c-transparenter-hintergrund.png)
:quality(80)/images.vogel.de/vogelonline/bdb/1330700/1330788/original.jpg)
:quality(80)/images.vogel.de/vogelonline/bdb/1330700/1330789/original.jpg)
:quality(80)/images.vogel.de/vogelonline/bdb/1330700/1330790/original.jpg)
:quality(80)/images.vogel.de/vogelonline/bdb/1330700/1330792/original.jpg)
:quality(80)/p7i.vogel.de/wcms/bf/30/bf3038b92e4988d6c883c155ef727153/0130924147v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/f5/ea/f5ea9b22a7e3774b8ca8a19e9db95915/0130921215v9.jpeg)